Transformările gazului ideal sunt procesele în care un gaz își... Afișează mai mult
Înscrie-te pentru a vedea CONȚINUTULE gratuit!
Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Knowunity AI
Mai mult
Materii
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Afișează toate materiile
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Afișează toate materiile
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Afișează toate materiile
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Afișează toate materiile
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Afișează toate materiile
71
•
Actualizat May 20, 2026
•
maia
@maiacrcl
Transformările gazului ideal sunt procesele în care un gaz își... Afișează mai mult
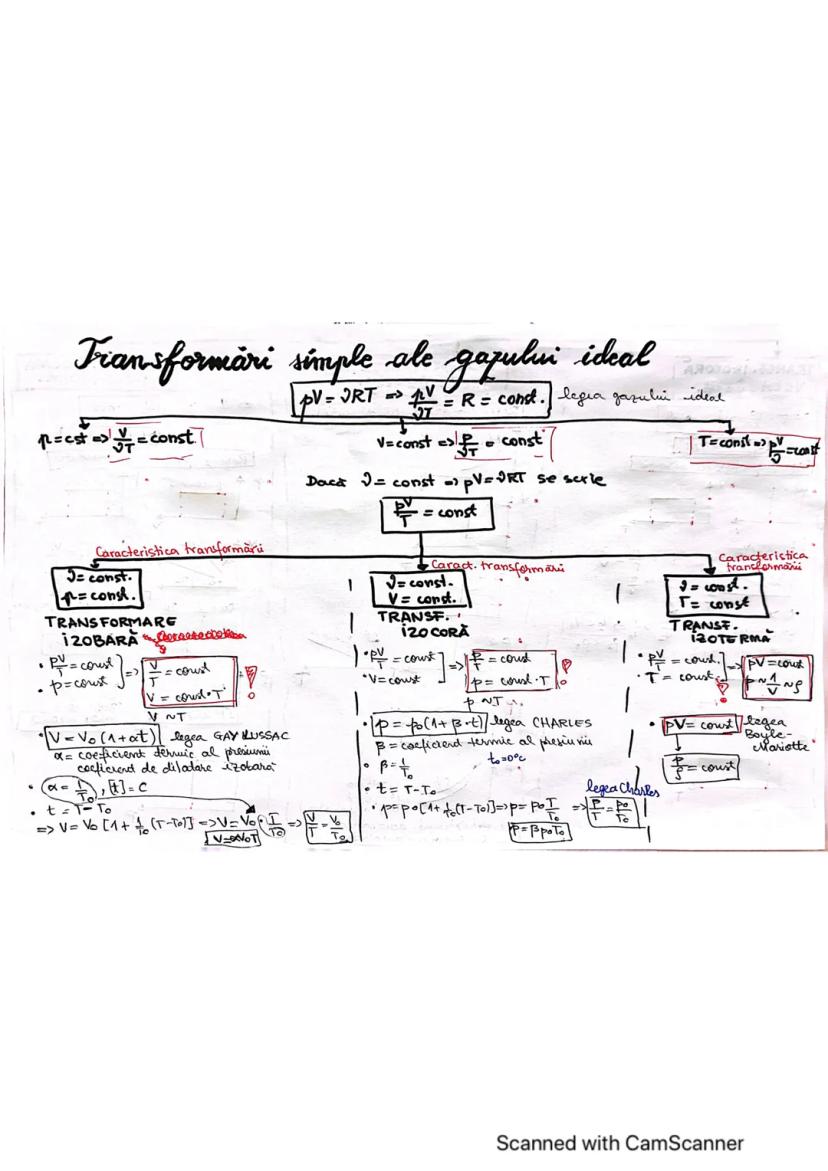







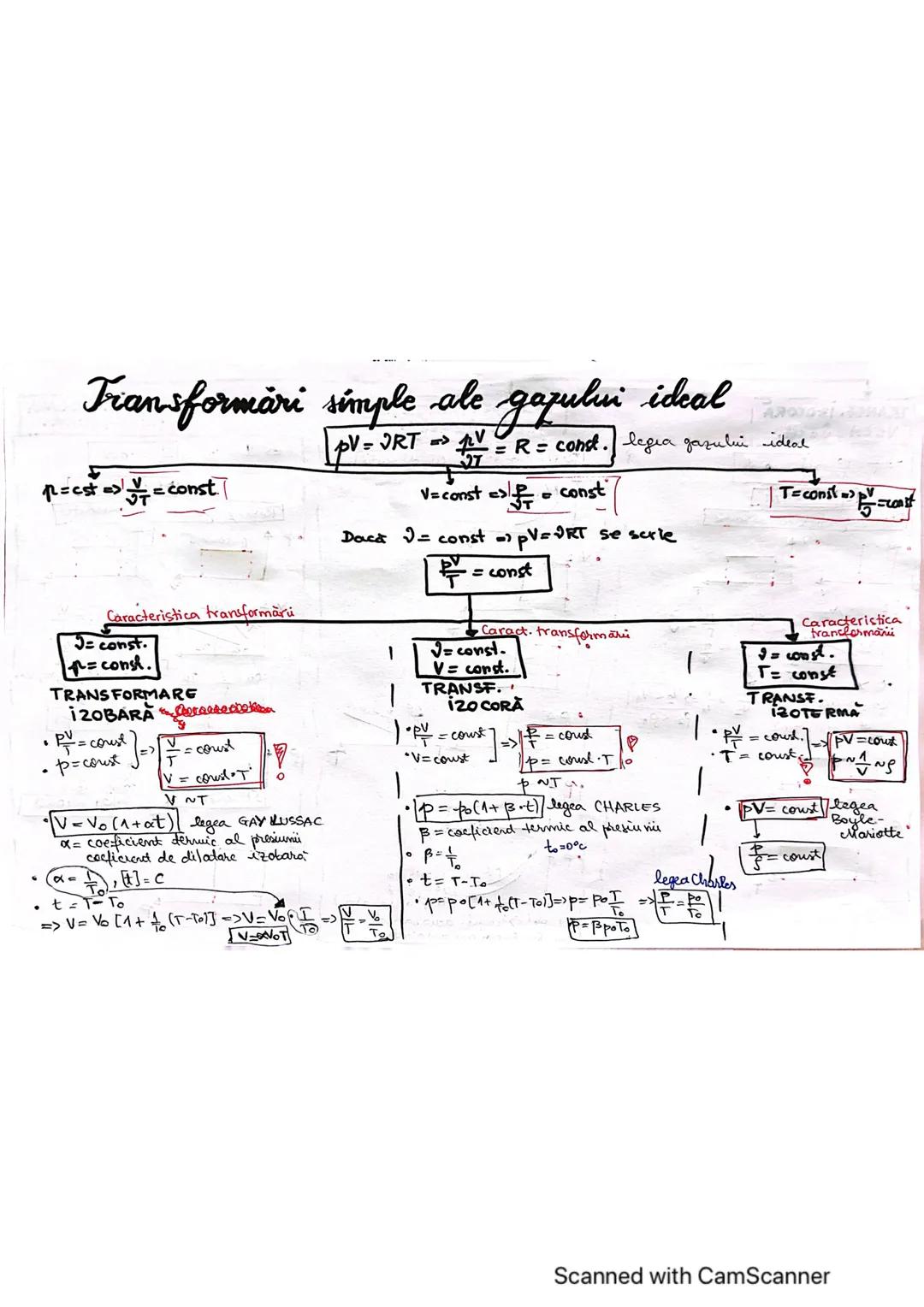
În transformarea izocorică volumul rămâne constant, iar presiunea și temperatura se modifică proporțional. Relația matematică care descrie această transformare este: p/T = p₀/T₀ = constant.
Când reprezentăm grafic transformarea izocorică, observăm că panta graficului depinde de volum - cu cât volumul este mai mic, cu atât panta este mai mare. Matematic, tangenta unghiului este tgα = V/T = nR/p, deci tgα ~ 1/p.
Atenție! În transformarea izocorică, lucrul mecanic este zero deoarece volumul nu se modifică .
În transformarea izotermă temperatura rămâne constantă, astfel pV = constant . Similar, în transformarea izobară presiunea rămâne constantă și obținem relația V/T = constant.
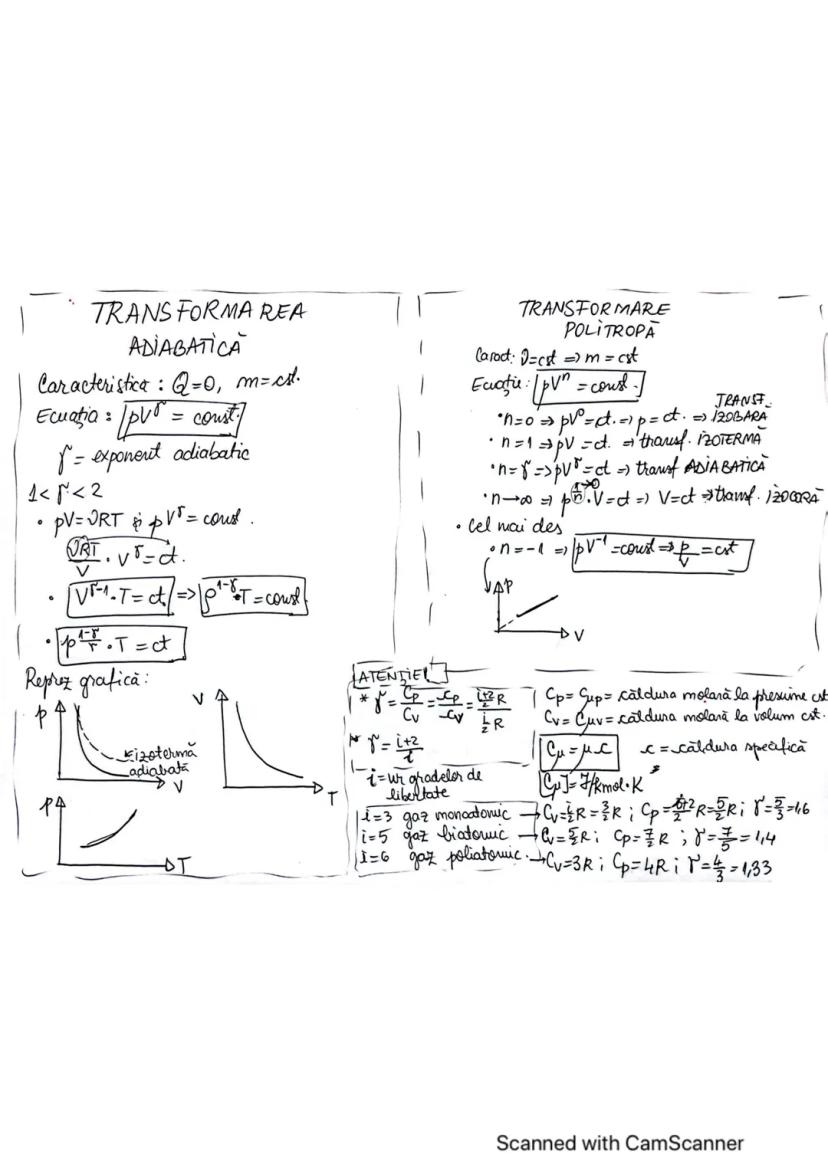
Pentru transformarea adiabatică, în care nu există schimb de căldură cu exteriorul, relația este pVᵞ = constant, unde γ este exponentul adiabatic și are valoarea γ > 1.

Când lucrăm cu gaze, avem nevoie de câteva concepte esențiale. Masa moleculară (m₀) este masa unei molecule măsurată în kg, iar numărul lui Avogadro (NA) reprezintă numărul de molecule dintr-un mol: NA = 6,023 · 10²³ molecule/mol.
Cantitatea de substanță (ν) este o mărime fizică fundamentală măsurată în moli. Alte concepte importante includ concentrația (n) care reprezintă numărul de molecule per volum, și numărul lui Loschmidt (n₀) care este concentrația unui gaz în condiții normale.
Important! În condiții normale de presiune și temperatură , volumul molar al oricărui gaz ideal este V₀ = 22,42·10⁻³ m³/mol.
Constanta universală a gazelor și constanta lui Boltzmann sunt legate prin relația k·NA = R. Presiunea se măsoară în Pascal (Pa) și poate fi convertită în alte unități: 1 atm = 1,013·10⁵ Pa, 1 torr = 133 Pa.

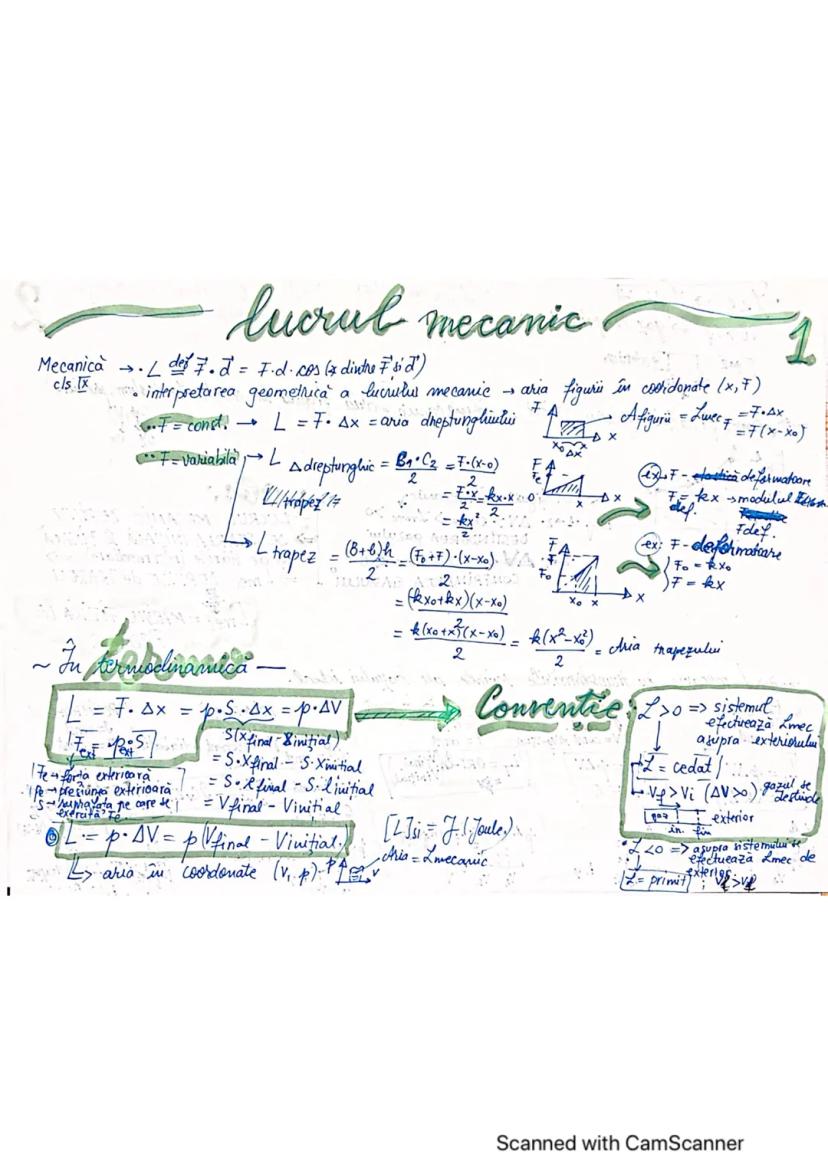
Lucrul mecanic în termeni geometrici reprezintă aria figurii în coordonate (V, p). Când un gaz este comprimat (Vᵢ > Vf), lucrul mecanic este negativ, iar când se destinde (Vᵢ < Vf), lucrul mecanic este pozitiv.
Un aspect important: lucrul mecanic depinde nu doar de stările inițială și finală, ci și de traseul urmat - este o mărime de proces, nu de stare.
În transformarea izobară , lucrul mecanic este L = p·ΔV. Pentru transformarea izocorică , lucrul mecanic este zero deoarece ΔV = 0.
De reținut! În transformarea izotermă , lucrul mecanic se calculează cu formula L = nRT·ln.
Pentru transformarea adiabatică , lucrul mecanic se exprimă ca L = nR/(1-γ), unde γ este exponentul adiabatic. În acest caz, căldura schimbată este zero .
În transformarea politropă , lucrul mecanic se calculează ca L = /, unde n este exponentul politropic.

Căldura (Q) este o mărime fizică de proces care reprezintă energia schimbată de sistem cu mediul exterior prin contact termic. Ea depinde de stările intermediare prin care evoluează sistemul și se măsoară în Jouli (J).
Prin convenție, căldura primită de sistem are valori pozitive (Q > 0), iar cea cedată are valori negative (Q < 0). Formula generală pentru calculul căldurii este Q = m·c·ΔT pentru solide și lichide, respectiv Q = ν·Cv·ΔT pentru gaze.
Bine de știut! Capacitatea calorică a unui corp (C) reprezintă cantitatea de căldură necesară pentru a modifica temperatura corpului cu 1 Kelvin.
Coeficienții calorici sunt mărimi fizice ce caracterizează proprietățile termice ale substanțelor:
Capacitatea calorică este o proprietate a corpului, în timp ce căldura specifică este o caracteristică a substanței din care este făcut corpul.

Căldura specifică (c) reprezintă căldura necesară unui kilogram de substanță pentru a-și modifica temperatura cu 1K. Relația dintre căldura molară și cea specifică este: Cᵤ = c·M, unde M este masa molară.
În cazul gazelor ideale, căldura molară la volum constant este Cv = ·R, iar la presiune constantă este Cp = ·R, unde i este numărul de grade de libertate. Exponentul adiabatic γ se calculează ca raportul γ = Cp/Cv = /i > 1.
Sfat util! Memorează formulele pentru căldura schimbată în fiecare tip de transformare, sunt esențiale pentru rezolvarea problemelor!
Iată cum calculăm căldura în transformările simple:
Pentru cazul special când n = -1 în transformarea politropă, avem relația p/V = constant.





Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
Aplicația este disponibilă în Google Play Store și Apple App Store.
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
App Store
Google Play
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS
maia
@maiacrcl
Transformările gazului ideal sunt procesele în care un gaz își modifică starea. În notițele următoare vom explora caracteristicile principalelor transformări, lucrul mecanic și transferul de căldură care au loc în aceste procese. Aceste concepte sunt fundamentale pentru înțelegerea termodinamicii și... Afișează mai mult

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
În transformarea izocorică volumul rămâne constant, iar presiunea și temperatura se modifică proporțional. Relația matematică care descrie această transformare este: p/T = p₀/T₀ = constant.
Când reprezentăm grafic transformarea izocorică, observăm că panta graficului depinde de volum - cu cât volumul este mai mic, cu atât panta este mai mare. Matematic, tangenta unghiului este tgα = V/T = nR/p, deci tgα ~ 1/p.
Atenție! În transformarea izocorică, lucrul mecanic este zero deoarece volumul nu se modifică .
În transformarea izotermă temperatura rămâne constantă, astfel pV = constant . Similar, în transformarea izobară presiunea rămâne constantă și obținem relația V/T = constant.
Pentru transformarea adiabatică, în care nu există schimb de căldură cu exteriorul, relația este pVᵞ = constant, unde γ este exponentul adiabatic și are valoarea γ > 1.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Când lucrăm cu gaze, avem nevoie de câteva concepte esențiale. Masa moleculară (m₀) este masa unei molecule măsurată în kg, iar numărul lui Avogadro (NA) reprezintă numărul de molecule dintr-un mol: NA = 6,023 · 10²³ molecule/mol.
Cantitatea de substanță (ν) este o mărime fizică fundamentală măsurată în moli. Alte concepte importante includ concentrația (n) care reprezintă numărul de molecule per volum, și numărul lui Loschmidt (n₀) care este concentrația unui gaz în condiții normale.
Important! În condiții normale de presiune și temperatură , volumul molar al oricărui gaz ideal este V₀ = 22,42·10⁻³ m³/mol.
Constanta universală a gazelor și constanta lui Boltzmann sunt legate prin relația k·NA = R. Presiunea se măsoară în Pascal (Pa) și poate fi convertită în alte unități: 1 atm = 1,013·10⁵ Pa, 1 torr = 133 Pa.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Lucrul mecanic în termeni geometrici reprezintă aria figurii în coordonate (V, p). Când un gaz este comprimat (Vᵢ > Vf), lucrul mecanic este negativ, iar când se destinde (Vᵢ < Vf), lucrul mecanic este pozitiv.
Un aspect important: lucrul mecanic depinde nu doar de stările inițială și finală, ci și de traseul urmat - este o mărime de proces, nu de stare.
În transformarea izobară , lucrul mecanic este L = p·ΔV. Pentru transformarea izocorică , lucrul mecanic este zero deoarece ΔV = 0.
De reținut! În transformarea izotermă , lucrul mecanic se calculează cu formula L = nRT·ln.
Pentru transformarea adiabatică , lucrul mecanic se exprimă ca L = nR/(1-γ), unde γ este exponentul adiabatic. În acest caz, căldura schimbată este zero .
În transformarea politropă , lucrul mecanic se calculează ca L = /, unde n este exponentul politropic.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Căldura (Q) este o mărime fizică de proces care reprezintă energia schimbată de sistem cu mediul exterior prin contact termic. Ea depinde de stările intermediare prin care evoluează sistemul și se măsoară în Jouli (J).
Prin convenție, căldura primită de sistem are valori pozitive (Q > 0), iar cea cedată are valori negative (Q < 0). Formula generală pentru calculul căldurii este Q = m·c·ΔT pentru solide și lichide, respectiv Q = ν·Cv·ΔT pentru gaze.
Bine de știut! Capacitatea calorică a unui corp (C) reprezintă cantitatea de căldură necesară pentru a modifica temperatura corpului cu 1 Kelvin.
Coeficienții calorici sunt mărimi fizice ce caracterizează proprietățile termice ale substanțelor:
Capacitatea calorică este o proprietate a corpului, în timp ce căldura specifică este o caracteristică a substanței din care este făcut corpul.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Căldura specifică (c) reprezintă căldura necesară unui kilogram de substanță pentru a-și modifica temperatura cu 1K. Relația dintre căldura molară și cea specifică este: Cᵤ = c·M, unde M este masa molară.
În cazul gazelor ideale, căldura molară la volum constant este Cv = ·R, iar la presiune constantă este Cp = ·R, unde i este numărul de grade de libertate. Exponentul adiabatic γ se calculează ca raportul γ = Cp/Cv = /i > 1.
Sfat util! Memorează formulele pentru căldura schimbată în fiecare tip de transformare, sunt esențiale pentru rezolvarea problemelor!
Iată cum calculăm căldura în transformările simple:
Pentru cazul special când n = -1 în transformarea politropă, avem relația p/V = constant.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
Aplicația este disponibilă în Google Play Store și Apple App Store.
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
3
Instrumente inteligente NOU
Transformă această notiță în: ✓ 50+ întrebări de exersare ✓ Flashcard-uri interactive ✓ Examen de practică complet ✓ Planuri de eseu
App Store
Google Play
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS