Termodinamica studiază comportamentul sistemelor fizice din perspectiva fenomenelor termice și... Afișează mai mult
Termodinamica pentru Admitere la Medicină - Partea 1









Fenomene termice și sisteme termodinamice
Fenomenele termice se bazează pe agitația termică - mișcarea continuă și spontană a particulelor în orice stare de agregare. Cu cât temperatura este mai mare, cu atât agitația este mai intensă. Un exemplu fascinant este mișcarea browniană - mișcarea dezordonată a particulelor microscopice în suspensie într-un lichid.
Un sistem termodinamic reprezintă un corp sau un ansamblu de corpuri cu un număr mare dar finit de particule. Tot ce nu face parte din sistem se numește mediu. Sistemele pot fi închise (nu schimbă substanță, dar pot schimba energie) sau deschise (schimbă substanță). De asemenea, pot fi izolate (nu schimbă nici energie, nici substanță) sau neizolate (fac schimburi).
Starea sistemului este definită de totalitatea proprietăților sale, măsurabile prin parametri de stare (precum presiune, volum, temperatură). Parametrii pot fi intensivi (nu depind de mărimea sistemului, ca P, T) sau extensivi (depind de mărimea sistemului, ca V, număr de moli).
💡 Când parametrii unui sistem nu se modifică în timp, sistemul se află în stare de echilibru - o stare fundamentală în termodinamică.
Procesele (sau transformările) reprezintă trecerea sistemului dintr-o stare în alta și pot fi: cvazistatice (lente) sau necvazistatice (bruște); deschise sau ciclice (închise); reversibile sau ireversibile.

Mărimi fizice fundamentale în termodinamică
Termodinamica utilizează mai multe mărimi fizice esențiale pentru descrierea sistemelor. Unitatea atomică de masă (notată u sau μ) este definită ca 1/12 din masa unui atom de carbon-12. Structura atomului include:
- Numărul de masă (A) = numărul de nucleoni
- Numărul atomic (Z) = numărul de electroni = numărul de protoni
Masa atomică/moleculară relativă reprezintă raportul dintre masa atomului/moleculei și unitatea atomică de masă. De exemplu, pentru apă (H₂O), masa moleculară relativă este suma maselor atomice relative: 2 × M<sub>H</sub> + M<sub>O</sub>. Câteva exemple utile:
- Masa atomică relativă a carbonului = 12
- Masa moleculară relativă a O₂ = 16 × 2 = 32
- 1 u.a.m. ≈ 1,67 × 10⁻²⁷ kg
💡 Atomii și moleculele sunt atât de mici încât e imposibil să le numărăm individual. De aceea folosim conceptul de mol - o unitate care ne permite să lucrăm cu cantități macroscopice.
Molul este cantitatea de substanță care conține un număr de particule (atomi, ioni sau molecule) egal cu numărul lui Avogadro (N<sub>A</sub> = 6,023 × 10²³ particule/mol). Masa molară reprezintă masa unui mol de substanță și se măsoară în g/mol .

Cantități de substanță și calcule
În termodinamică, sunt esențiale relațiile dintre numărul de particule, masa și cantitatea de substanță. Masa molară se determină adunând masele atomice relative ale elementelor componente. De exemplu:
- Pentru apă (H₂O): M<sub>ml</sub> = 2 × M<sub>H</sub> + M<sub>O</sub> = 2 × 1 + 16 = 18 g/mol
- Pentru oxigen (O₂): M<sub>ml</sub> = 32 g/mol
Numărul de moli (ν) dintr-o cantitate de substanță poate fi calculat în mai multe moduri:
ν = m/μ = N/N<sub>A</sub> = V/V<sub>μ</sub>
unde:
- m este masa substanței
- μ este masa molară
- N este numărul de molecule
- N<sub>A</sub> este numărul lui Avogadro
- V este volumul (pentru gaze)
- V<sub>μ</sub> este volumul molar
💡 Pentru a determina numărul de molecule dintr-o cantitate de substanță, poți folosi formula: N = (m × N<sub>A</sub>)/μ
Pentru a calcula masa unei molecule, împarți masa molară la numărul lui Avogadro: m<sub>0</sub> = μ/N<sub>A</sub>. De exemplu, pentru CO₂ , masa unei molecule este: m<sub>0</sub> = 44/(6,023 × 10²³) ≈ 7,3 × 10⁻²³ g.

Prefixe și unități de măsură în termodinamică
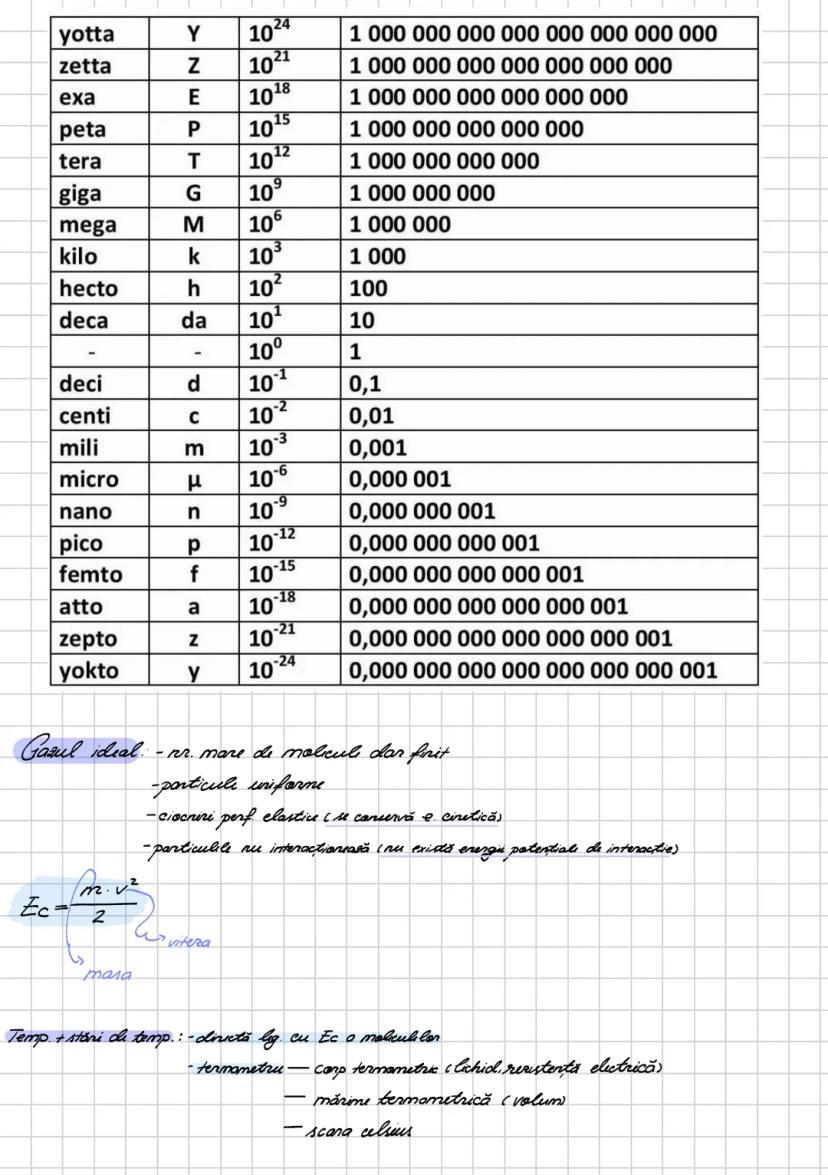
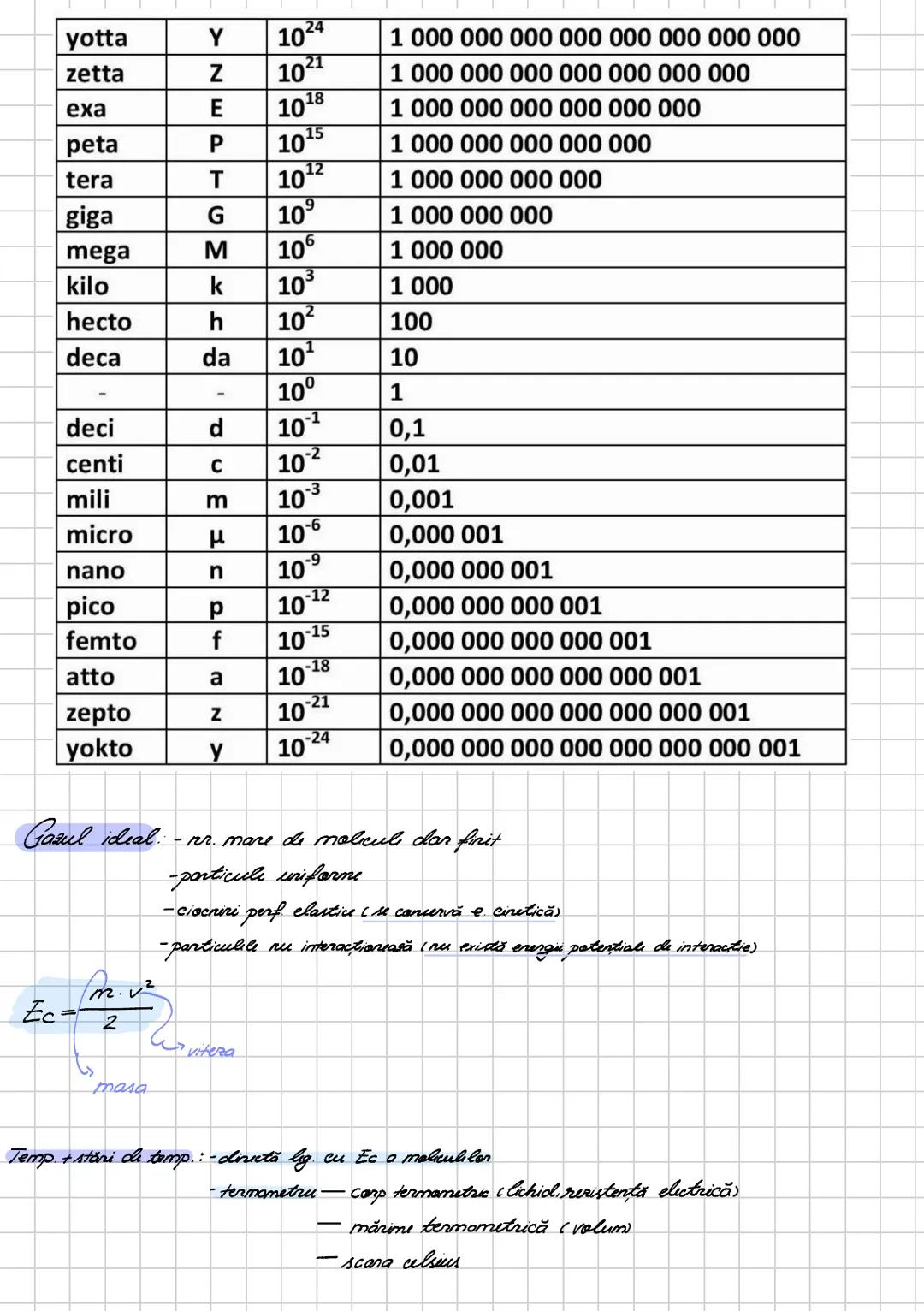
În termodinamică folosim adesea valori foarte mari sau foarte mici, de aceea e important să stăpânești prefixele unităților de măsură. Cele mai frecvent utilizate sunt:
- kilo (k) = 10³
- mega (M) = 10⁶
- giga (G) = 10⁹
- mili (m) = 10⁻³
- micro (μ) = 10⁻⁶
- nano (n) = 10⁻⁹
Gazul ideal este un model teoretic care ne ajută să înțelegem comportamentul gazelor reale. Un gaz ideal are următoarele caracteristici:
- Conține un număr mare dar finit de molecule uniforme
- Ciocnirile dintre particule sunt perfect elastice (energia cinetică se conservă)
- Particulele nu interacționează între ele (nu există energie potențială de interacție)
💡 Modelul gazului ideal este o aproximare, dar este extrem de util pentru a înțelege legile gazelor și pentru a face calcule precise în majoritatea situațiilor practice.
Temperatura este direct legată de energia cinetică a moleculelor. Pentru măsurarea temperaturii folosim un termometru cu corp termometric (lichid sau rezistență electrică). Pe scara Celsius, punctul de îngheț al apei la presiune normală este 0°C, iar punctul de fierbere este 100°C.
Presiunea și legile hidrostatice
Presiunea reprezintă forța exercitată perpendicular pe unitatea de suprafață și se măsoară în Pascal (Pa) = N/m². Presiunea normală atmosferică este 1 atm = 1,013 × 10⁵ Pa.
Legea lui Pascal afirmă că presiunea exercitată asupra unui lichid se transmite cu aceeași intensitate în toată masa lichidului. Aceasta explică cum funcționează sistemele hidraulice, de la frânele mașinii până la elevatoarele hidraulice.
Presiunea hidrostatică într-un lichid crește cu adâncimea conform formulei: P = P₀ + ρgh
unde:
- P₀ este presiunea atmosferică
- ρ este densitatea lichidului
- g este accelerația gravitațională
- h este adâncimea
💡 Principiul fundamental al hidrostaticii stabilește că într-un lichid aflat în echilibru, presiunea în puncte de egală adâncime are aceeași valoare în toate direcțiile. Acest principiu este esențial pentru înțelegerea plutirii corpurilor și a modului în care funcționează barometrele și manometrele.
Aceste concepte de hidrostatică sunt strâns legate de termodinamică, deoarece presiunea este unul dintre parametrii fundamentali care definesc starea unui sistem termodinamic, fiind esențială în studiul gazelor și al transformărilor termodinamice.

Noțiuni și relații fundamentale în termodinamică
În termodinamică, există câteva relații esențiale pe care trebuie să le înțelegi bine. Relația dintre constanta universală a gazelor (R), numărul lui Avogadro (N<sub>A</sub>) și constanta lui Boltzmann (k) este: R = N<sub>A</sub> × k.
Molul este unitatea de măsură pentru cantitatea de substanță și conține întotdeauna N<sub>A</sub> particule, indiferent de tipul substanței. Masa molară depinde de tipul substanței și se exprimă în g/mol.
Pentru a determina numărul de moli dintr-un sistem, poți folosi oricare dintre aceste relații:
- ν = m/μ
- ν = N/N<sub>A</sub>
- ν = V/V<sub>μ</sub>
💡 Transformările cvasistatice sunt procese lente în care sistemul trece prin stări succesive de echilibru. Acestea pot fi reprezentate grafic și sunt esențiale pentru înțelegerea motoarelor termice și a eficienței lor.
În sistemele de gaze, presiunea exercitată de un gaz ideal în echilibru termodinamic este aceeași pe toți pereții vasului și este determinată de ciocnirile moleculelor cu pereții. Viteza termică a moleculelor depinde atât de temperatură, cât și de natura gazului. Două gaze diferite aflate în echilibru termic au aceeași temperatură și aceeași energie cinetică medie per moleculă.



Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut: First Law of Thermodynamics
3Cel mai popular conținut la Matematică
9EN CLASA a6
Evaluarea națională pentru clasa a-6-a matematica fizica și biologie
Fizica Electricitate
formule cu mici explicatii
Formule Mecanica BAC
Formule pentru BAC la Fizica - Mecanica
Materie optica-admitere medicina
Toata materia necesara pt capitolul de optica✨
Termodinamica-materie admitere medicina
Tot capitolul de termodinamica pentru admiterea la medicina!✨
MECANICA
PROGRAMA DE BACALAUREAT PENTRU MECANICA
Materie electricitate-admitere medicina
Toata materia de la capitolul de electricitate pentru admitere la facultatea de medicina✨
Electricitate -Teoremele lui Kirchhoff
Teoremele lui Kirchhoff
Evaluarea Națională 2024-2025
clasa a 6-a
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Termodinamica pentru Admitere la Medicină - Partea 1
Termodinamica studiază comportamentul sistemelor fizice din perspectiva fenomenelor termice și a relațiilor dintre căldură, lucru mecanic și alte forme de energie. Aceste concepte ne ajută să înțelegem lumea din jurul nostru, de la cum funcționează motoarele până la procesele care... Afișează mai mult

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Fenomene termice și sisteme termodinamice
Fenomenele termice se bazează pe agitația termică - mișcarea continuă și spontană a particulelor în orice stare de agregare. Cu cât temperatura este mai mare, cu atât agitația este mai intensă. Un exemplu fascinant este mișcarea browniană - mișcarea dezordonată a particulelor microscopice în suspensie într-un lichid.
Un sistem termodinamic reprezintă un corp sau un ansamblu de corpuri cu un număr mare dar finit de particule. Tot ce nu face parte din sistem se numește mediu. Sistemele pot fi închise (nu schimbă substanță, dar pot schimba energie) sau deschise (schimbă substanță). De asemenea, pot fi izolate (nu schimbă nici energie, nici substanță) sau neizolate (fac schimburi).
Starea sistemului este definită de totalitatea proprietăților sale, măsurabile prin parametri de stare (precum presiune, volum, temperatură). Parametrii pot fi intensivi (nu depind de mărimea sistemului, ca P, T) sau extensivi (depind de mărimea sistemului, ca V, număr de moli).
💡 Când parametrii unui sistem nu se modifică în timp, sistemul se află în stare de echilibru - o stare fundamentală în termodinamică.
Procesele (sau transformările) reprezintă trecerea sistemului dintr-o stare în alta și pot fi: cvazistatice (lente) sau necvazistatice (bruște); deschise sau ciclice (închise); reversibile sau ireversibile.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Mărimi fizice fundamentale în termodinamică
Termodinamica utilizează mai multe mărimi fizice esențiale pentru descrierea sistemelor. Unitatea atomică de masă (notată u sau μ) este definită ca 1/12 din masa unui atom de carbon-12. Structura atomului include:
- Numărul de masă (A) = numărul de nucleoni
- Numărul atomic (Z) = numărul de electroni = numărul de protoni
Masa atomică/moleculară relativă reprezintă raportul dintre masa atomului/moleculei și unitatea atomică de masă. De exemplu, pentru apă (H₂O), masa moleculară relativă este suma maselor atomice relative: 2 × M<sub>H</sub> + M<sub>O</sub>. Câteva exemple utile:
- Masa atomică relativă a carbonului = 12
- Masa moleculară relativă a O₂ = 16 × 2 = 32
- 1 u.a.m. ≈ 1,67 × 10⁻²⁷ kg
💡 Atomii și moleculele sunt atât de mici încât e imposibil să le numărăm individual. De aceea folosim conceptul de mol - o unitate care ne permite să lucrăm cu cantități macroscopice.
Molul este cantitatea de substanță care conține un număr de particule (atomi, ioni sau molecule) egal cu numărul lui Avogadro (N<sub>A</sub> = 6,023 × 10²³ particule/mol). Masa molară reprezintă masa unui mol de substanță și se măsoară în g/mol .

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Cantități de substanță și calcule
În termodinamică, sunt esențiale relațiile dintre numărul de particule, masa și cantitatea de substanță. Masa molară se determină adunând masele atomice relative ale elementelor componente. De exemplu:
- Pentru apă (H₂O): M<sub>ml</sub> = 2 × M<sub>H</sub> + M<sub>O</sub> = 2 × 1 + 16 = 18 g/mol
- Pentru oxigen (O₂): M<sub>ml</sub> = 32 g/mol
Numărul de moli (ν) dintr-o cantitate de substanță poate fi calculat în mai multe moduri:
ν = m/μ = N/N<sub>A</sub> = V/V<sub>μ</sub>
unde:
- m este masa substanței
- μ este masa molară
- N este numărul de molecule
- N<sub>A</sub> este numărul lui Avogadro
- V este volumul (pentru gaze)
- V<sub>μ</sub> este volumul molar
💡 Pentru a determina numărul de molecule dintr-o cantitate de substanță, poți folosi formula: N = (m × N<sub>A</sub>)/μ
Pentru a calcula masa unei molecule, împarți masa molară la numărul lui Avogadro: m<sub>0</sub> = μ/N<sub>A</sub>. De exemplu, pentru CO₂ , masa unei molecule este: m<sub>0</sub> = 44/(6,023 × 10²³) ≈ 7,3 × 10⁻²³ g.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Prefixe și unități de măsură în termodinamică
În termodinamică folosim adesea valori foarte mari sau foarte mici, de aceea e important să stăpânești prefixele unităților de măsură. Cele mai frecvent utilizate sunt:
- kilo (k) = 10³
- mega (M) = 10⁶
- giga (G) = 10⁹
- mili (m) = 10⁻³
- micro (μ) = 10⁻⁶
- nano (n) = 10⁻⁹
Gazul ideal este un model teoretic care ne ajută să înțelegem comportamentul gazelor reale. Un gaz ideal are următoarele caracteristici:
- Conține un număr mare dar finit de molecule uniforme
- Ciocnirile dintre particule sunt perfect elastice (energia cinetică se conservă)
- Particulele nu interacționează între ele (nu există energie potențială de interacție)
💡 Modelul gazului ideal este o aproximare, dar este extrem de util pentru a înțelege legile gazelor și pentru a face calcule precise în majoritatea situațiilor practice.
Temperatura este direct legată de energia cinetică a moleculelor. Pentru măsurarea temperaturii folosim un termometru cu corp termometric (lichid sau rezistență electrică). Pe scara Celsius, punctul de îngheț al apei la presiune normală este 0°C, iar punctul de fierbere este 100°C.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Presiunea și legile hidrostatice
Presiunea reprezintă forța exercitată perpendicular pe unitatea de suprafață și se măsoară în Pascal (Pa) = N/m². Presiunea normală atmosferică este 1 atm = 1,013 × 10⁵ Pa.
Legea lui Pascal afirmă că presiunea exercitată asupra unui lichid se transmite cu aceeași intensitate în toată masa lichidului. Aceasta explică cum funcționează sistemele hidraulice, de la frânele mașinii până la elevatoarele hidraulice.
Presiunea hidrostatică într-un lichid crește cu adâncimea conform formulei: P = P₀ + ρgh
unde:
- P₀ este presiunea atmosferică
- ρ este densitatea lichidului
- g este accelerația gravitațională
- h este adâncimea
💡 Principiul fundamental al hidrostaticii stabilește că într-un lichid aflat în echilibru, presiunea în puncte de egală adâncime are aceeași valoare în toate direcțiile. Acest principiu este esențial pentru înțelegerea plutirii corpurilor și a modului în care funcționează barometrele și manometrele.
Aceste concepte de hidrostatică sunt strâns legate de termodinamică, deoarece presiunea este unul dintre parametrii fundamentali care definesc starea unui sistem termodinamic, fiind esențială în studiul gazelor și al transformărilor termodinamice.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Noțiuni și relații fundamentale în termodinamică
În termodinamică, există câteva relații esențiale pe care trebuie să le înțelegi bine. Relația dintre constanta universală a gazelor (R), numărul lui Avogadro (N<sub>A</sub>) și constanta lui Boltzmann (k) este: R = N<sub>A</sub> × k.
Molul este unitatea de măsură pentru cantitatea de substanță și conține întotdeauna N<sub>A</sub> particule, indiferent de tipul substanței. Masa molară depinde de tipul substanței și se exprimă în g/mol.
Pentru a determina numărul de moli dintr-un sistem, poți folosi oricare dintre aceste relații:
- ν = m/μ
- ν = N/N<sub>A</sub>
- ν = V/V<sub>μ</sub>
💡 Transformările cvasistatice sunt procese lente în care sistemul trece prin stări succesive de echilibru. Acestea pot fi reprezentate grafic și sunt esențiale pentru înțelegerea motoarelor termice și a eficienței lor.
În sistemele de gaze, presiunea exercitată de un gaz ideal în echilibru termodinamic este aceeași pe toți pereții vasului și este determinată de ciocnirile moleculelor cu pereții. Viteza termică a moleculelor depinde atât de temperatură, cât și de natura gazului. Două gaze diferite aflate în echilibru termic au aceeași temperatură și aceeași energie cinetică medie per moleculă.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut: First Law of Thermodynamics
3Cel mai popular conținut la Matematică
9EN CLASA a6
Evaluarea națională pentru clasa a-6-a matematica fizica și biologie
Fizica Electricitate
formule cu mici explicatii
Formule Mecanica BAC
Formule pentru BAC la Fizica - Mecanica
Materie optica-admitere medicina
Toata materia necesara pt capitolul de optica✨
Termodinamica-materie admitere medicina
Tot capitolul de termodinamica pentru admiterea la medicina!✨
MECANICA
PROGRAMA DE BACALAUREAT PENTRU MECANICA
Materie electricitate-admitere medicina
Toata materia de la capitolul de electricitate pentru admitere la facultatea de medicina✨
Electricitate -Teoremele lui Kirchhoff
Teoremele lui Kirchhoff
Evaluarea Națională 2024-2025
clasa a 6-a
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.