Fizica gazelor ideale este un subiect fascinant care ne ajută... Afișează mai mult
Introducere în Termodinamica - Lecție pentru Clasa a X-a





Cantitatea de substanță și ecuația de stare a gazului
Numărul de moli reprezintă cantitatea de substanță și se calculează prin formula: m = N/NA = V/Vμ, unde N este numărul de molecule și NA este numărul lui Avogadro .
În condiții normale de temperatură (0°C) și presiune , volumul molar normal al unui mol de substanță este de 22,42·10⁻³ m³/mol.
Ecuația termică de stare a gazelor ideale este pV = νRT, unde p este presiunea, V este volumul, ν este numărul de moli, T este temperatura absolută și R este constanta universală a gazelor .
💡 Un gaz ideal este un model teoretic perfect al unui gaz real. În realitate, niciun gaz nu e perfect ideal, dar la presiuni mici și temperaturi ridicate, multe gaze se comportă aproape ideal!

Energia internă și formula fundamentală a T.C.M.
Concentrația gazului se definește ca n = N/V, reprezentând numărul de molecule per unitate de volum. Temperatura se măsoară în Kelvin (unitate fundamentală), cu relația simplă: T(K) = t(°C) + 273.
Formula fundamentală a Teoriei Cinetico-Moleculare (T.C.M.) este p = (2/3)·n·, stabilind legătura dintre presiune și energia cinetică a moleculelor.
Energia internă a gazului ideal este dată de formula U = ·νRT, unde i reprezintă numărul gradelor de libertate: i=3 pentru gaz monoatomic (He), i=5 pentru gaz biatomic (O₂, N₂), și i=6 pentru gaz pluriatomic (CO₂).
🔍 Constanta lui Boltzmann face legătura între lumea macroscopică și cea microscopică, fiind raportul dintre constanta gazelor R și numărul lui Avogadro.

Transformări simple ale gazului ideal
În cazul coloanelor de fluid în repaus, presiunea se calculează cu formula P = ρgh, unde ρ este densitatea, g este accelerația gravitațională și h este înălțimea coloanei.
Transformarea izotermă are loc la temperatură constantă: PV = constant sau P₁V₁ = P₂V₂. Graficul acesteia este o hiperbolă în coordonate P-V.
Transformarea izobară are loc la presiune constantă: V/T = constant sau V = V₀, unde α este coeficientul de dilatare și V₀ este volumul la 0°C.
Transformarea izocoră (Charles) are loc la volum constant: P/T = constant sau P = P₀, unde β este coeficientul termic al presiunii și P₀ este presiunea la 0°C.
💡 Memorează relația dintre cele trei transformări simple prin inițialele TIP: T(emperatură) pentru izotermă, I(presiune) pentru izobară și P(volum) pentru izocoră!

Transformări și mărimi termodinamice
Transformarea generală a gazului ideal (la masă constantă) respectă legea: PV/T = constant.
Energia internă (U) este o mărime de stare, funcție doar de temperatură: U = νRT. Este o mărime scalară aditivă și se măsoară în Joule.
Căldura (Q) reprezintă o formă de schimb de energie. Este pozitivă când este primită și negativă când este cedată de sistem. Căldura este o mărime de proces, nu de stare.
Lucrul mecanic (L) este tot o mărime de proces, măsurată în Joule. L > 0 în cazul destinderii (volumul final > volumul inițial) și L < 0 în cazul comprimării (Vf < Vi).
🔑 Diferența crucială: energia internă este o mărime de stare (depinde doar de starea inițială și finală), în timp ce căldura și lucrul mecanic sunt mărimi de proces (depind de calea urmată)!
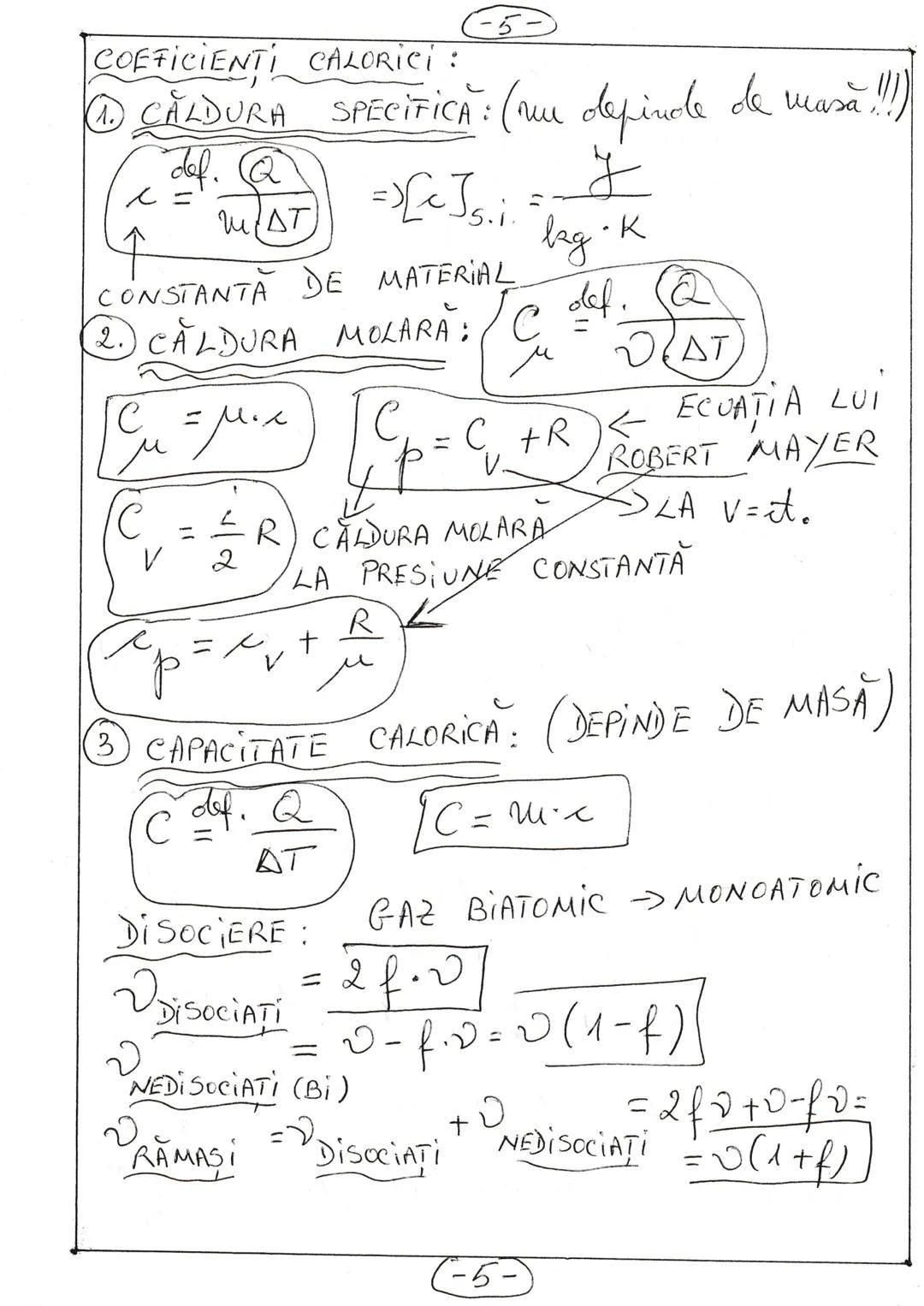
Coeficienți calorici și disocierea gazelor
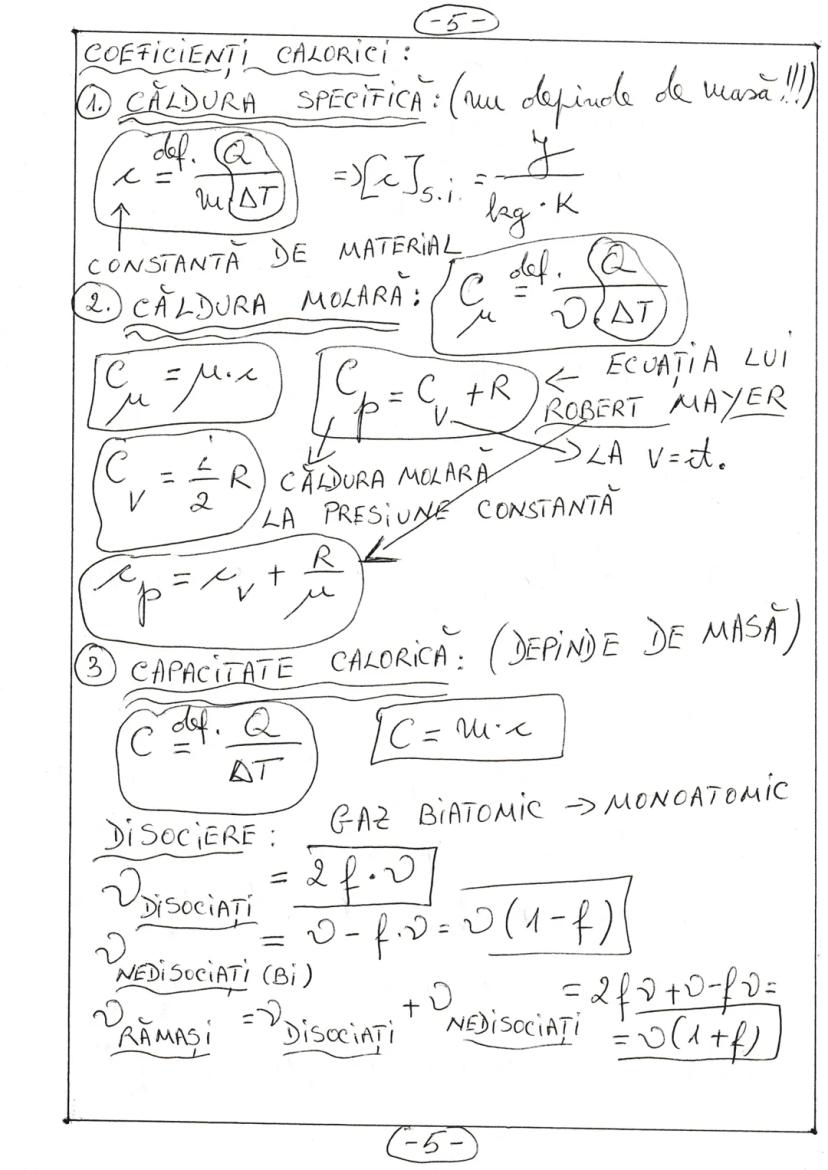
Căldura specifică (c) definită ca c = Q/(m·ΔT) este o constantă de material și se măsoară în J/(kg·K).
Căldura molară (Cμ) se calculează ca Cμ = μ·c = Q/(ν·ΔT), unde μ este masa molară. Ecuația lui Robert Mayer stabilește relația între căldura molară la presiune constantă și volum constant: Cp = Cv + R sau cp = cv + R/μ.
Capacitatea calorică (C) depinde de masă și se definește ca C = Q/ΔT = m·c.
În cazul disocierii unui gaz biatomic în gaz monoatomic, dacă ν este numărul inițial de moli și f este gradul de disociere, atunci numărul total de moli după disociere este ν, cu ν·f moli disociați și ν moli nedisociați.
📝 Căldurile molare depind de structura gazului: cu cât molecula are mai multe grade de libertate, cu atât poate stoca mai multă energie și are o căldură molară mai mare!
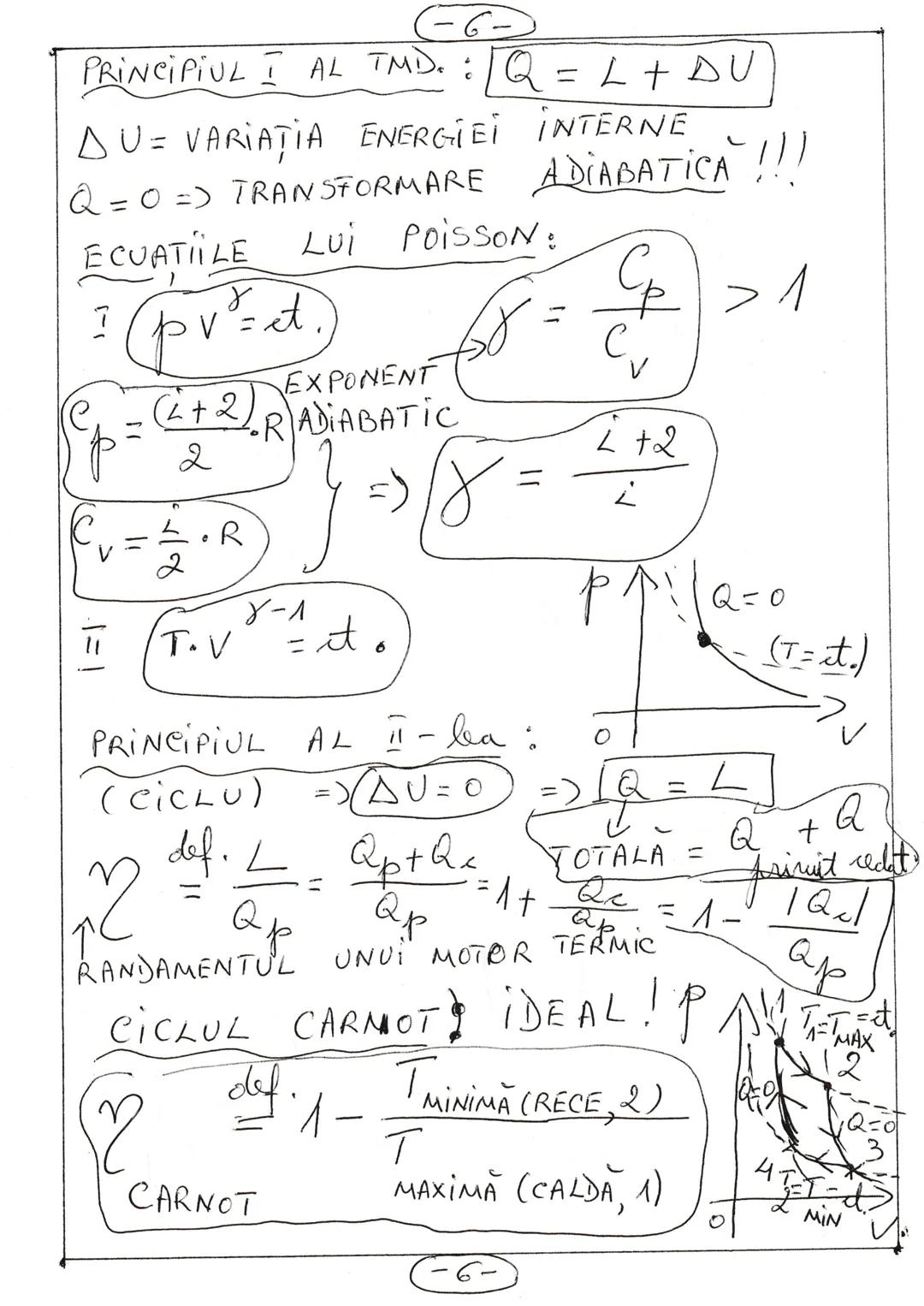
Principiile termodinamicii și ciclul Carnot
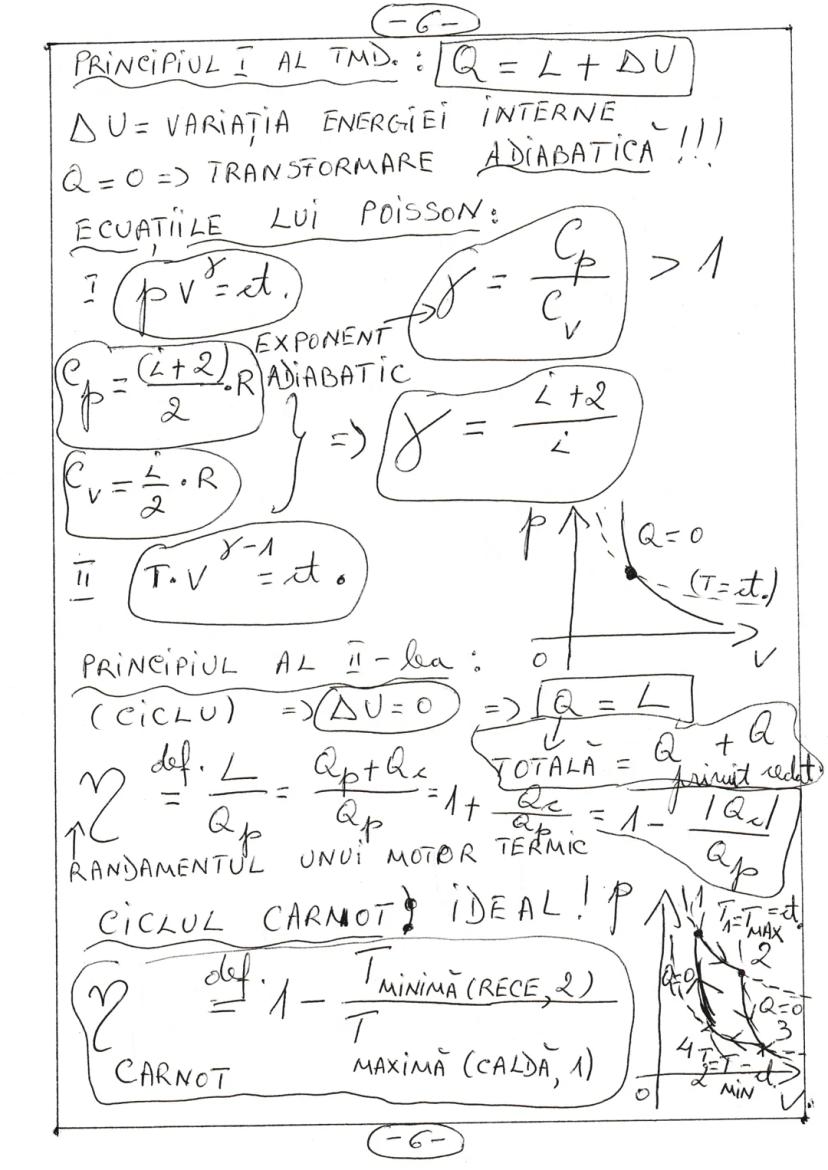
Principiul I al termodinamicii stabilește că: Q = L + ΔU, unde ΔU este variația energiei interne. În transformarea adiabatică Q = 0, deci L = -ΔU.
Ecuațiile lui Poisson pentru transformarea adiabatică sunt: pVᵞ = constant și (T·V)ᵞ⁻¹ = constant, unde γ = Cp/Cv = /i este exponentul adiabatic.
Principiul al II-lea aplicat la cicluri termice permite calculul randamentului: η = L/Qp = 1 - |Qc|/Qp, unde Qp este căldura primită și Qc este căldura cedată.
Ciclul Carnot ideal are randamentul maxim teoretic: η = 1 - T₂/T₁, unde T₂ este temperatura sursei reci și T₁ este temperatura sursei calde.
🚀 Ciclul Carnot reprezintă standardul de aur în termodinamică - niciun motor termic real nu poate avea un randament mai mare decât un motor Carnot funcționând între aceleași temperaturi!
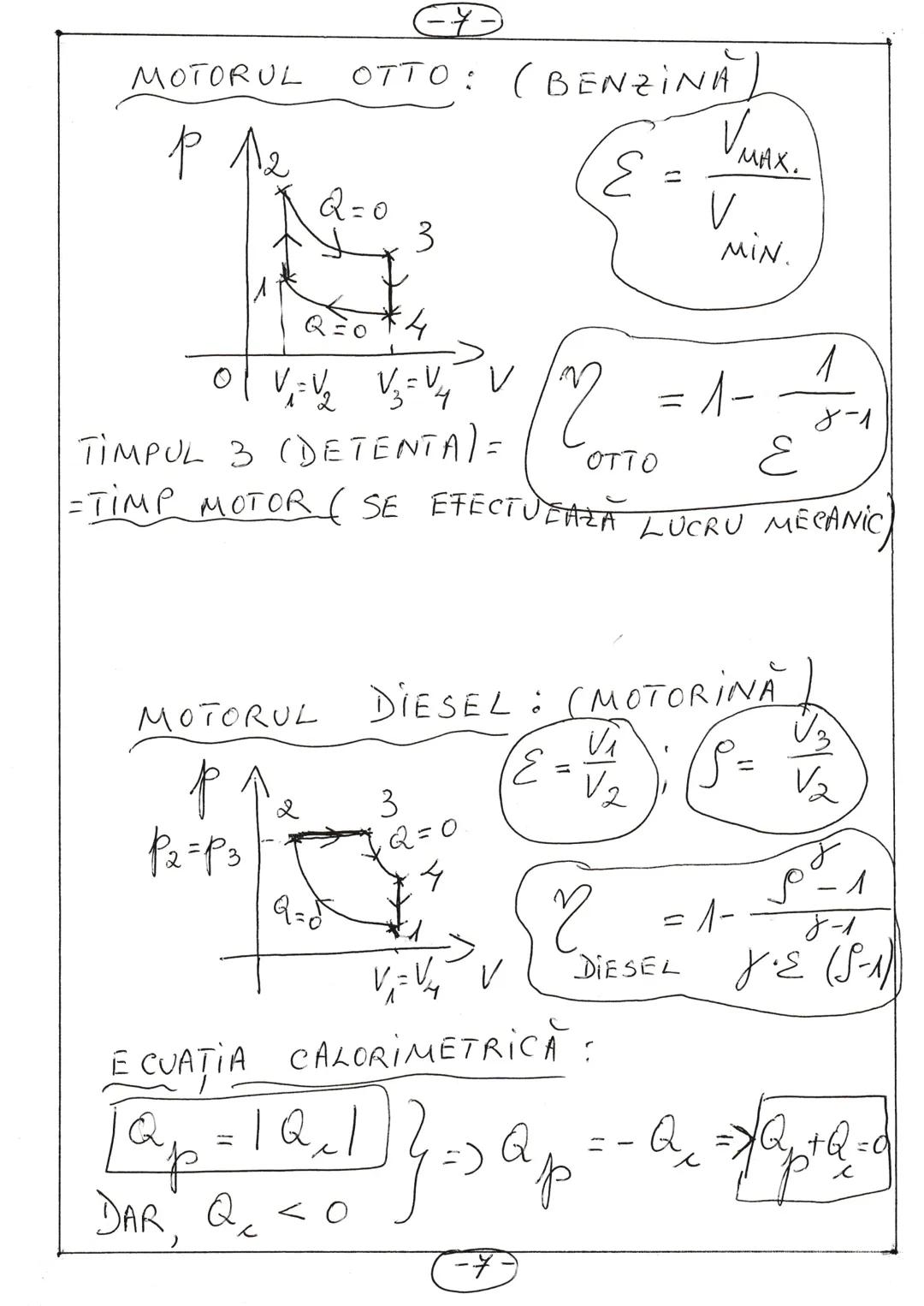
Motoarele termice: Otto și Diesel
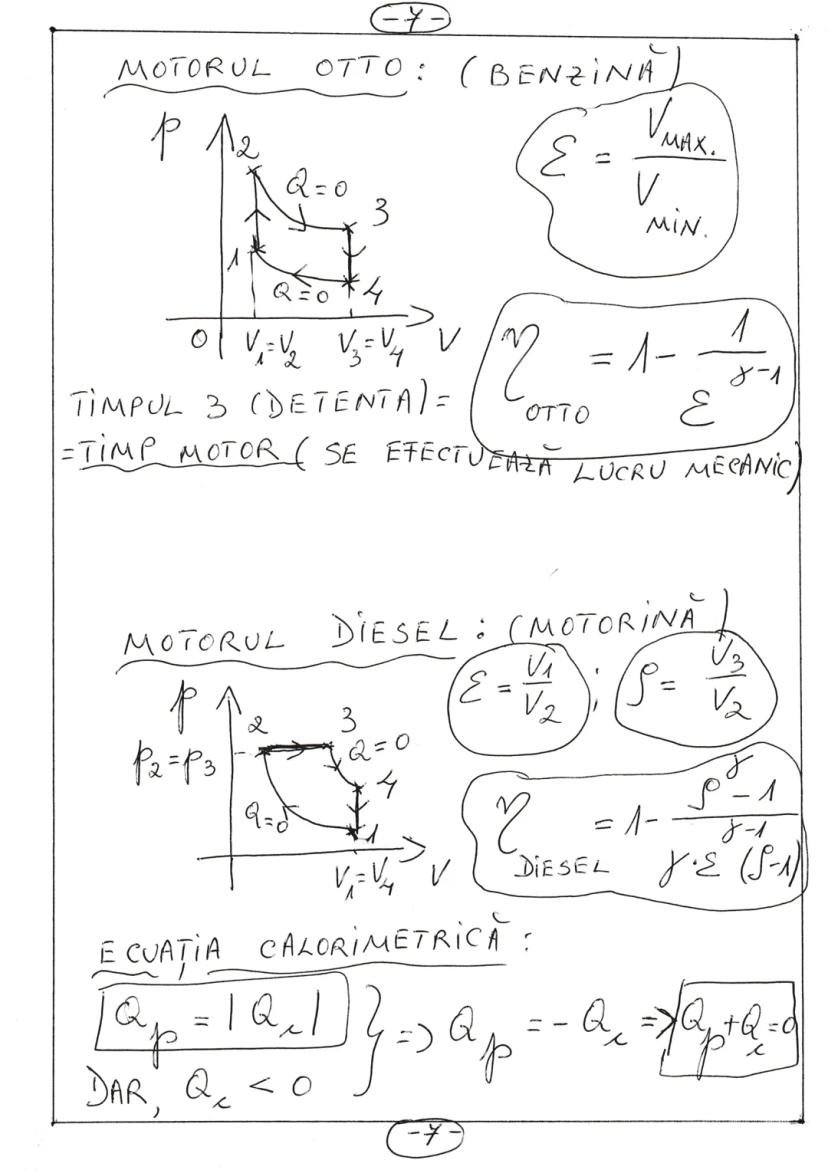
Motorul Otto (pe benzină) are un randament teoretic dat de formula: ηOtto = 1 - 1/εᵞ⁻¹, unde ε = Vmax/Vmin este raportul de compresie.
Ciclul Otto are patru timpi, dintre care timpul 3 (detenta) este timpul motor - momentul în care se efectuează lucru mecanic util.
Motorul Diesel (pe motorină) are randamentul teoretic: ηDiesel = 1 - ρᵞ⁻¹/[γ·ε·(ρ-1)], unde ε = V₁/V₂ este raportul de compresie și ρ = V₃/V₂ este raportul de destindere izobară.
Ecuația calorimetrică stabilește că într-un proces de schimb de căldură, căldura cedată de un corp este egală cu căldura primită de celălalt: |Qp| = |Qc| sau Qp + Qc = 0 (Qc fiind negativ).
🔥 Principala diferență dintre motoarele Otto și Diesel este modul de aprindere: Otto folosește bujii pentru aprindere, în timp ce Diesel folosește comprimarea puternică a aerului pentru a crește temperatura până la auto-aprindere!
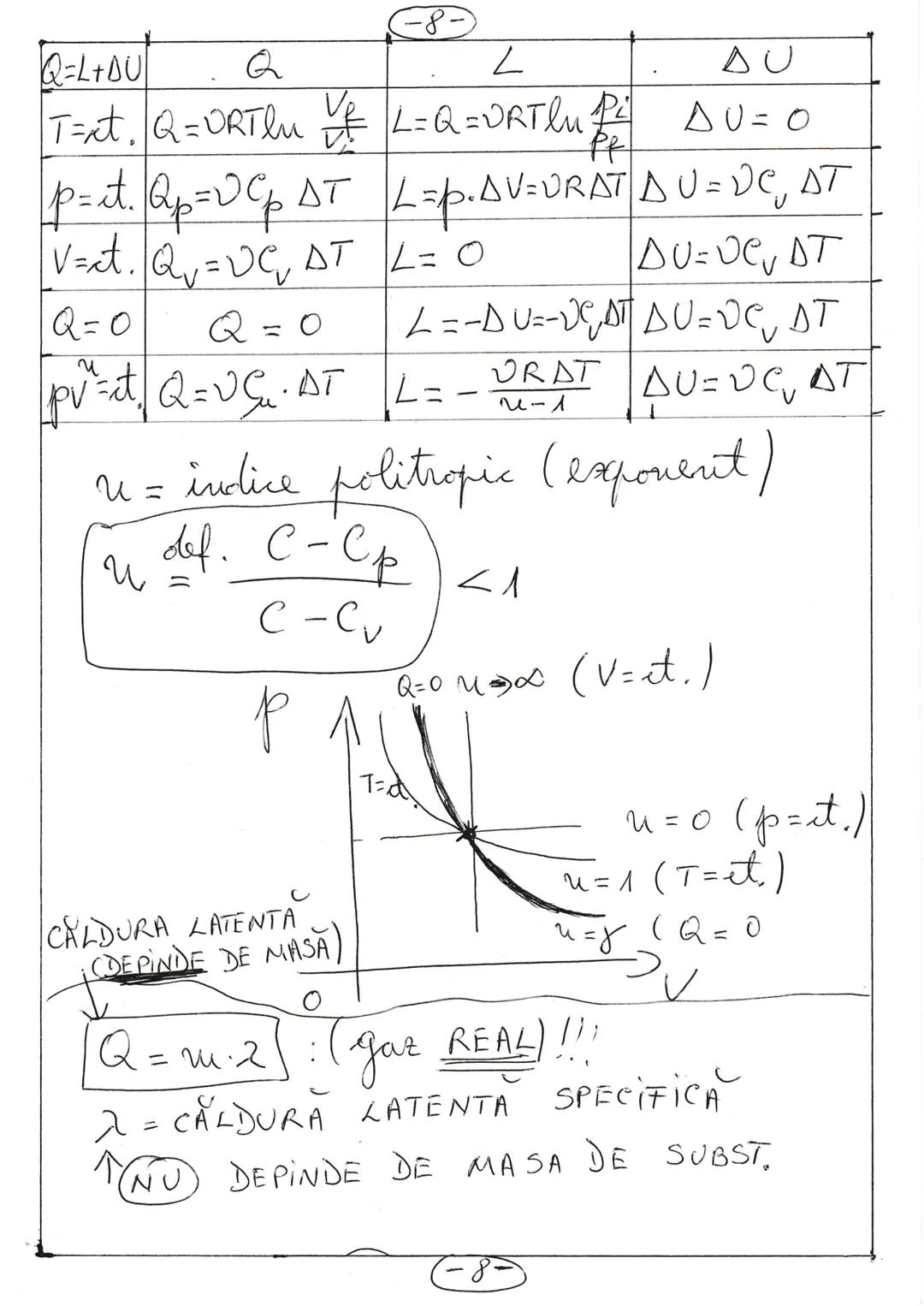
Transformările și căldura latentă
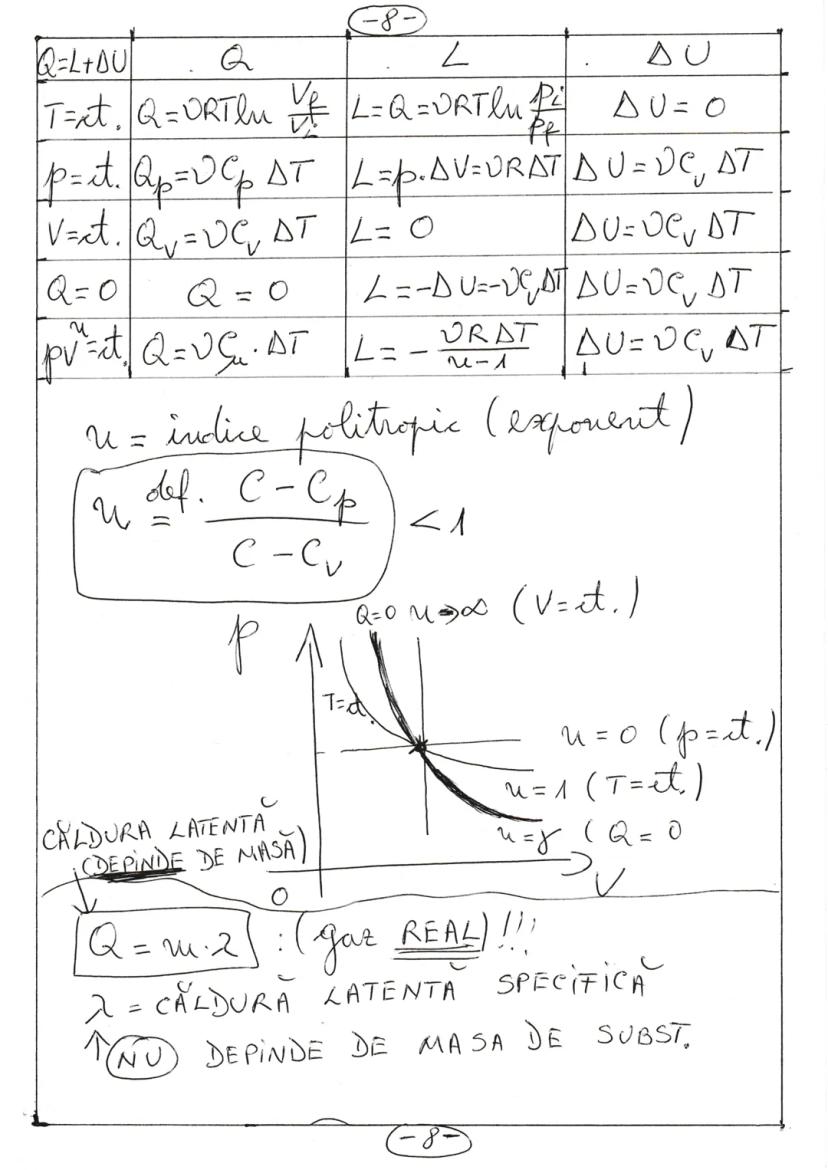
Pentru diferitele transformări ale gazelor ideale, relațiile dintre căldură (Q), lucru mecanic (L) și variația energiei interne (ΔU) sunt specifice:
- Izotermă : Q = νRTln, L = Q, ΔU = 0
- Izobară : Q = νCpΔT, L = pΔV = νRΔT, ΔU = νCvΔT
- Izocoră : Q = νCvΔT, L = 0, ΔU = Q
În transformarea politropică , indicele politropic u = / determină comportamentul transformării: u < 0 (Q < 0), u = 0 , u = 1 , u = γ .
Căldura latentă reprezintă căldura necesară pentru schimbarea stării de agregare a unei substanțe, unde λ este căldura latentă specifică, o proprietate a materialului care nu depinde de masă.
🧊 Când apa îngheață, eliberează aceeași cantitate de energie pe care ar trebui să o absoarbă pentru a se topi! De aceea, în sezonul rece, agricultorii stropesc plantele cu apă pentru a le proteja de îngheț.
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut la Matematică
9EN CLASA a6
Evaluarea națională pentru clasa a-6-a matematica fizica și biologie
Fizica Electricitate
formule cu mici explicatii
Formule Mecanica BAC
Formule pentru BAC la Fizica - Mecanica
Materie optica-admitere medicina
Toata materia necesara pt capitolul de optica✨
Termodinamica-materie admitere medicina
Tot capitolul de termodinamica pentru admiterea la medicina!✨
MECANICA
PROGRAMA DE BACALAUREAT PENTRU MECANICA
Materie electricitate-admitere medicina
Toata materia de la capitolul de electricitate pentru admitere la facultatea de medicina✨
Electricitate -Teoremele lui Kirchhoff
Teoremele lui Kirchhoff
Evaluarea Națională 2024-2025
clasa a 6-a
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Introducere în Termodinamica - Lecție pentru Clasa a X-a
Fizica gazelor ideale este un subiect fascinant care ne ajută să înțelegem comportamentul particulelor în stare gazoasă. Aceste note acoperă concepte fundamentale despre moli, presiune, energie internă și transformări de stare ale gazelor, fiind esențiale pentru a înțelege cum funcționează... Afișează mai mult

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Cantitatea de substanță și ecuația de stare a gazului
Numărul de moli reprezintă cantitatea de substanță și se calculează prin formula: m = N/NA = V/Vμ, unde N este numărul de molecule și NA este numărul lui Avogadro .
În condiții normale de temperatură (0°C) și presiune , volumul molar normal al unui mol de substanță este de 22,42·10⁻³ m³/mol.
Ecuația termică de stare a gazelor ideale este pV = νRT, unde p este presiunea, V este volumul, ν este numărul de moli, T este temperatura absolută și R este constanta universală a gazelor .
💡 Un gaz ideal este un model teoretic perfect al unui gaz real. În realitate, niciun gaz nu e perfect ideal, dar la presiuni mici și temperaturi ridicate, multe gaze se comportă aproape ideal!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Energia internă și formula fundamentală a T.C.M.
Concentrația gazului se definește ca n = N/V, reprezentând numărul de molecule per unitate de volum. Temperatura se măsoară în Kelvin (unitate fundamentală), cu relația simplă: T(K) = t(°C) + 273.
Formula fundamentală a Teoriei Cinetico-Moleculare (T.C.M.) este p = (2/3)·n·, stabilind legătura dintre presiune și energia cinetică a moleculelor.
Energia internă a gazului ideal este dată de formula U = ·νRT, unde i reprezintă numărul gradelor de libertate: i=3 pentru gaz monoatomic (He), i=5 pentru gaz biatomic (O₂, N₂), și i=6 pentru gaz pluriatomic (CO₂).
🔍 Constanta lui Boltzmann face legătura între lumea macroscopică și cea microscopică, fiind raportul dintre constanta gazelor R și numărul lui Avogadro.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Transformări simple ale gazului ideal
În cazul coloanelor de fluid în repaus, presiunea se calculează cu formula P = ρgh, unde ρ este densitatea, g este accelerația gravitațională și h este înălțimea coloanei.
Transformarea izotermă are loc la temperatură constantă: PV = constant sau P₁V₁ = P₂V₂. Graficul acesteia este o hiperbolă în coordonate P-V.
Transformarea izobară are loc la presiune constantă: V/T = constant sau V = V₀, unde α este coeficientul de dilatare și V₀ este volumul la 0°C.
Transformarea izocoră (Charles) are loc la volum constant: P/T = constant sau P = P₀, unde β este coeficientul termic al presiunii și P₀ este presiunea la 0°C.
💡 Memorează relația dintre cele trei transformări simple prin inițialele TIP: T(emperatură) pentru izotermă, I(presiune) pentru izobară și P(volum) pentru izocoră!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Transformări și mărimi termodinamice
Transformarea generală a gazului ideal (la masă constantă) respectă legea: PV/T = constant.
Energia internă (U) este o mărime de stare, funcție doar de temperatură: U = νRT. Este o mărime scalară aditivă și se măsoară în Joule.
Căldura (Q) reprezintă o formă de schimb de energie. Este pozitivă când este primită și negativă când este cedată de sistem. Căldura este o mărime de proces, nu de stare.
Lucrul mecanic (L) este tot o mărime de proces, măsurată în Joule. L > 0 în cazul destinderii (volumul final > volumul inițial) și L < 0 în cazul comprimării (Vf < Vi).
🔑 Diferența crucială: energia internă este o mărime de stare (depinde doar de starea inițială și finală), în timp ce căldura și lucrul mecanic sunt mărimi de proces (depind de calea urmată)!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Coeficienți calorici și disocierea gazelor
Căldura specifică (c) definită ca c = Q/(m·ΔT) este o constantă de material și se măsoară în J/(kg·K).
Căldura molară (Cμ) se calculează ca Cμ = μ·c = Q/(ν·ΔT), unde μ este masa molară. Ecuația lui Robert Mayer stabilește relația între căldura molară la presiune constantă și volum constant: Cp = Cv + R sau cp = cv + R/μ.
Capacitatea calorică (C) depinde de masă și se definește ca C = Q/ΔT = m·c.
În cazul disocierii unui gaz biatomic în gaz monoatomic, dacă ν este numărul inițial de moli și f este gradul de disociere, atunci numărul total de moli după disociere este ν, cu ν·f moli disociați și ν moli nedisociați.
📝 Căldurile molare depind de structura gazului: cu cât molecula are mai multe grade de libertate, cu atât poate stoca mai multă energie și are o căldură molară mai mare!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Principiile termodinamicii și ciclul Carnot
Principiul I al termodinamicii stabilește că: Q = L + ΔU, unde ΔU este variația energiei interne. În transformarea adiabatică Q = 0, deci L = -ΔU.
Ecuațiile lui Poisson pentru transformarea adiabatică sunt: pVᵞ = constant și (T·V)ᵞ⁻¹ = constant, unde γ = Cp/Cv = /i este exponentul adiabatic.
Principiul al II-lea aplicat la cicluri termice permite calculul randamentului: η = L/Qp = 1 - |Qc|/Qp, unde Qp este căldura primită și Qc este căldura cedată.
Ciclul Carnot ideal are randamentul maxim teoretic: η = 1 - T₂/T₁, unde T₂ este temperatura sursei reci și T₁ este temperatura sursei calde.
🚀 Ciclul Carnot reprezintă standardul de aur în termodinamică - niciun motor termic real nu poate avea un randament mai mare decât un motor Carnot funcționând între aceleași temperaturi!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Motoarele termice: Otto și Diesel
Motorul Otto (pe benzină) are un randament teoretic dat de formula: ηOtto = 1 - 1/εᵞ⁻¹, unde ε = Vmax/Vmin este raportul de compresie.
Ciclul Otto are patru timpi, dintre care timpul 3 (detenta) este timpul motor - momentul în care se efectuează lucru mecanic util.
Motorul Diesel (pe motorină) are randamentul teoretic: ηDiesel = 1 - ρᵞ⁻¹/[γ·ε·(ρ-1)], unde ε = V₁/V₂ este raportul de compresie și ρ = V₃/V₂ este raportul de destindere izobară.
Ecuația calorimetrică stabilește că într-un proces de schimb de căldură, căldura cedată de un corp este egală cu căldura primită de celălalt: |Qp| = |Qc| sau Qp + Qc = 0 (Qc fiind negativ).
🔥 Principala diferență dintre motoarele Otto și Diesel este modul de aprindere: Otto folosește bujii pentru aprindere, în timp ce Diesel folosește comprimarea puternică a aerului pentru a crește temperatura până la auto-aprindere!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Transformările și căldura latentă
Pentru diferitele transformări ale gazelor ideale, relațiile dintre căldură (Q), lucru mecanic (L) și variația energiei interne (ΔU) sunt specifice:
- Izotermă : Q = νRTln, L = Q, ΔU = 0
- Izobară : Q = νCpΔT, L = pΔV = νRΔT, ΔU = νCvΔT
- Izocoră : Q = νCvΔT, L = 0, ΔU = Q
În transformarea politropică , indicele politropic u = / determină comportamentul transformării: u < 0 (Q < 0), u = 0 , u = 1 , u = γ .
Căldura latentă reprezintă căldura necesară pentru schimbarea stării de agregare a unei substanțe, unde λ este căldura latentă specifică, o proprietate a materialului care nu depinde de masă.
🧊 Când apa îngheață, eliberează aceeași cantitate de energie pe care ar trebui să o absoarbă pentru a se topi! De aceea, în sezonul rece, agricultorii stropesc plantele cu apă pentru a le proteja de îngheț.
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut la Matematică
9EN CLASA a6
Evaluarea națională pentru clasa a-6-a matematica fizica și biologie
Fizica Electricitate
formule cu mici explicatii
Formule Mecanica BAC
Formule pentru BAC la Fizica - Mecanica
Materie optica-admitere medicina
Toata materia necesara pt capitolul de optica✨
Termodinamica-materie admitere medicina
Tot capitolul de termodinamica pentru admiterea la medicina!✨
MECANICA
PROGRAMA DE BACALAUREAT PENTRU MECANICA
Materie electricitate-admitere medicina
Toata materia de la capitolul de electricitate pentru admitere la facultatea de medicina✨
Electricitate -Teoremele lui Kirchhoff
Teoremele lui Kirchhoff
Evaluarea Națională 2024-2025
clasa a 6-a
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.