Legile gazelor ideale sunt fundamentul termodinamicii și explică comportamentul gazelor... Afișează mai mult
Legile Gazului în Termodinamică



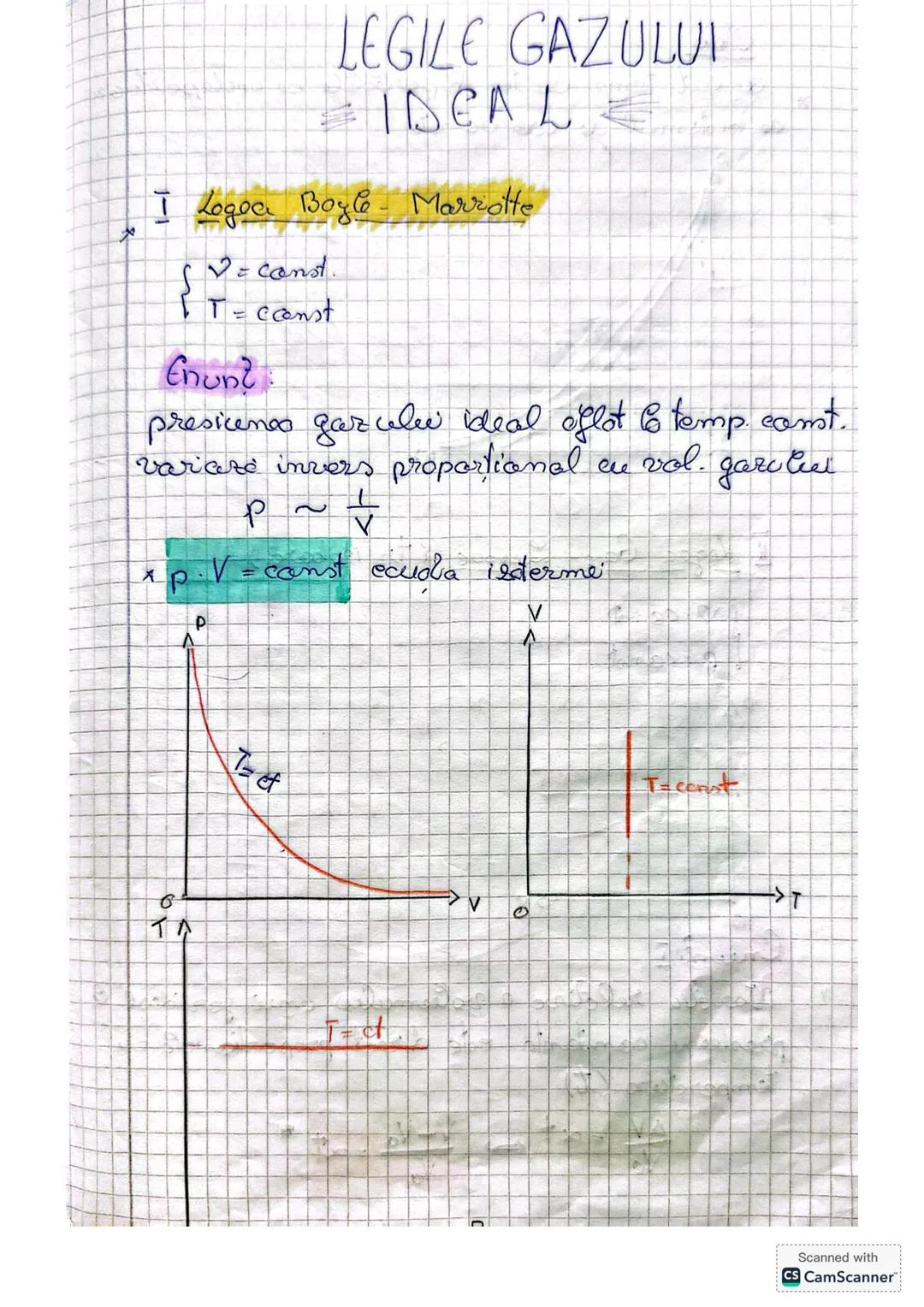
Legea Boyle-Mariotte (Transformarea izotermă)
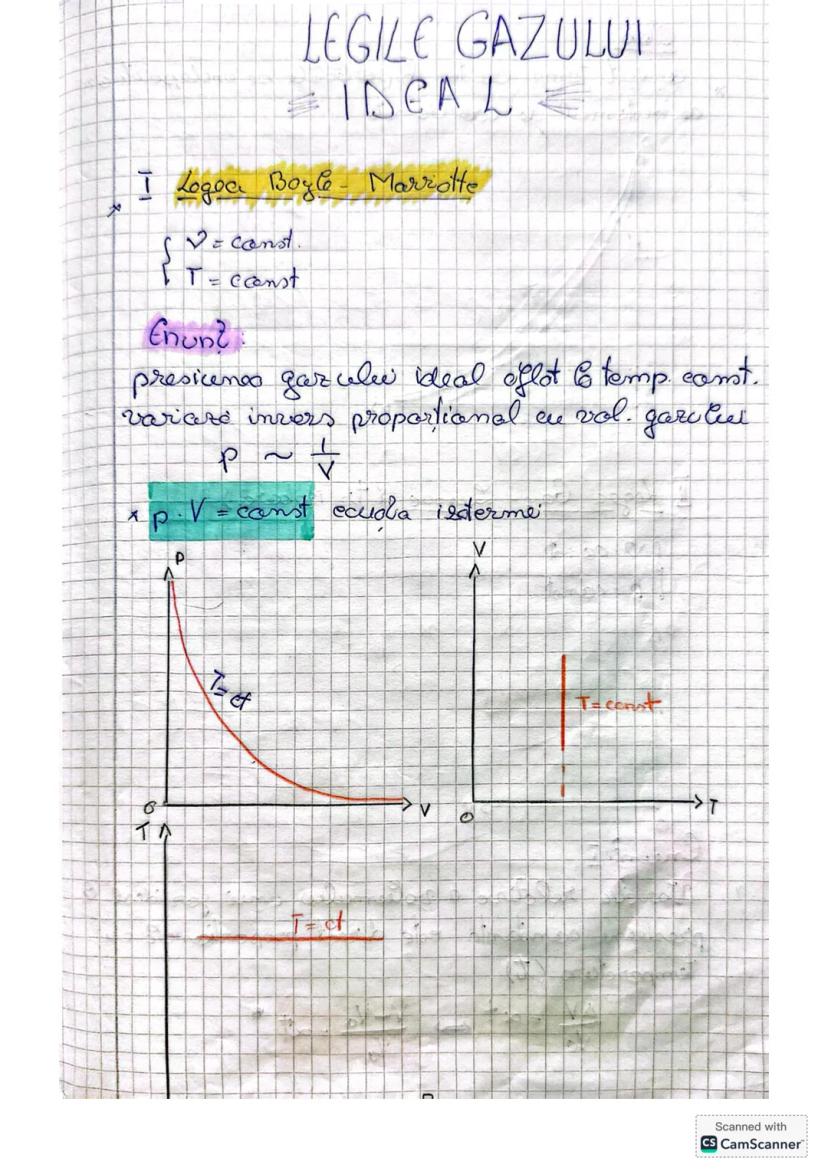
La temperatura constantă, presiunea unui gaz ideal variază invers proporțional cu volumul său. Adică, dacă volumul scade, presiunea crește și invers.
Formula matematică a acestei legi este foarte simplă: p·V = constant. Această ecuație descrie o izotermă, care grafic apare ca o hiperbolă.
Pe grafic, putem observa cum la volume mari presiunea este mică, iar când volumul scade, presiunea crește brusc. E ca atunci când comprimi aerul într-o pompă de bicicletă - simți cum devine din ce în ce mai greu să împingi!
💡 Când rezolvi probleme cu transformări izoterme, amintește-ți că produsul p·V rămâne același în orice punct al transformării.
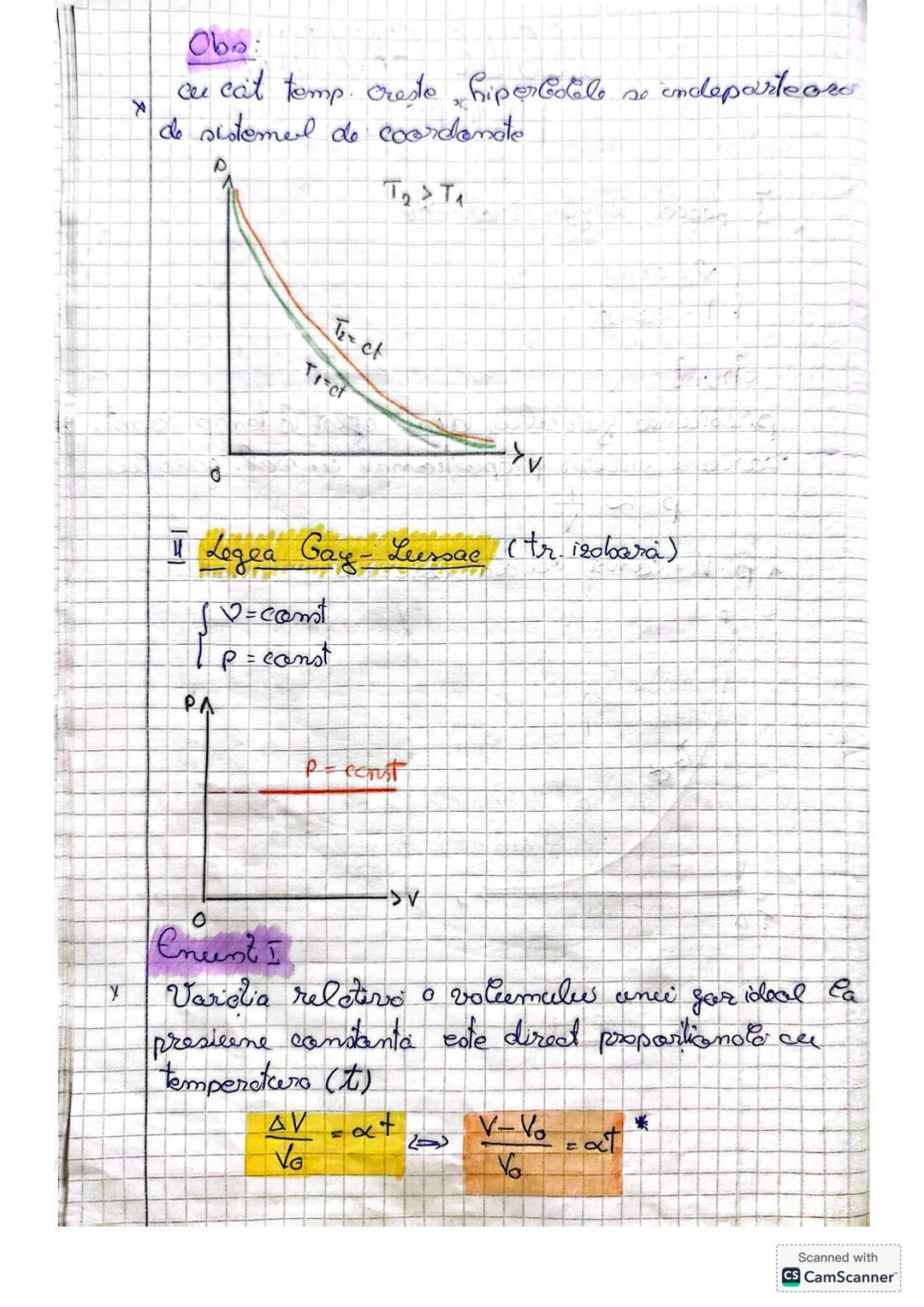
Legea Gay-Lussac (Transformarea izobară)
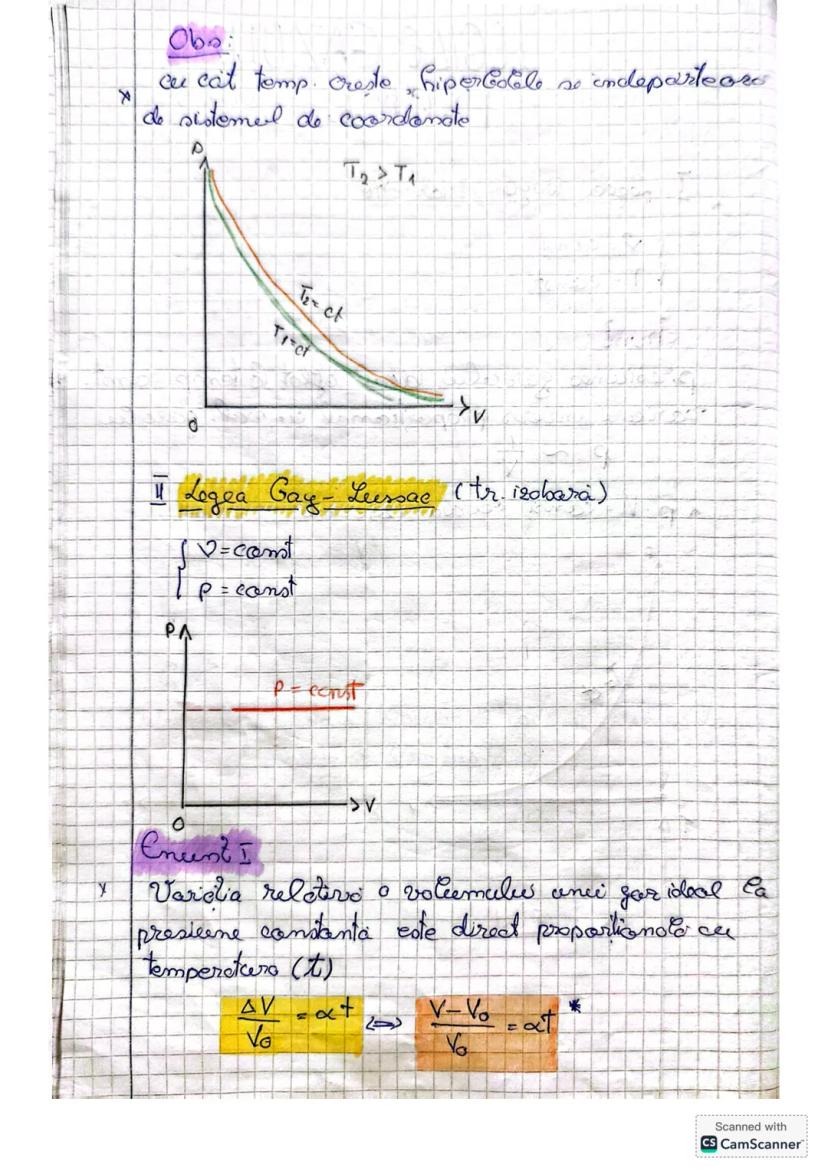
La presiune constantă, volumul unui gaz ideal variază direct proporțional cu temperatura. Când încălzești un gaz menținând presiunea constantă, acesta se dilată uniform.
Matematic, variația relativă a volumului se exprimă prin formula: /V₀ = α × t, unde V₀ este volumul la 0°C, iar α este coeficientul de dilatare termică volumară al gazului, egal cu aproximativ 1/273,15 K⁻¹.
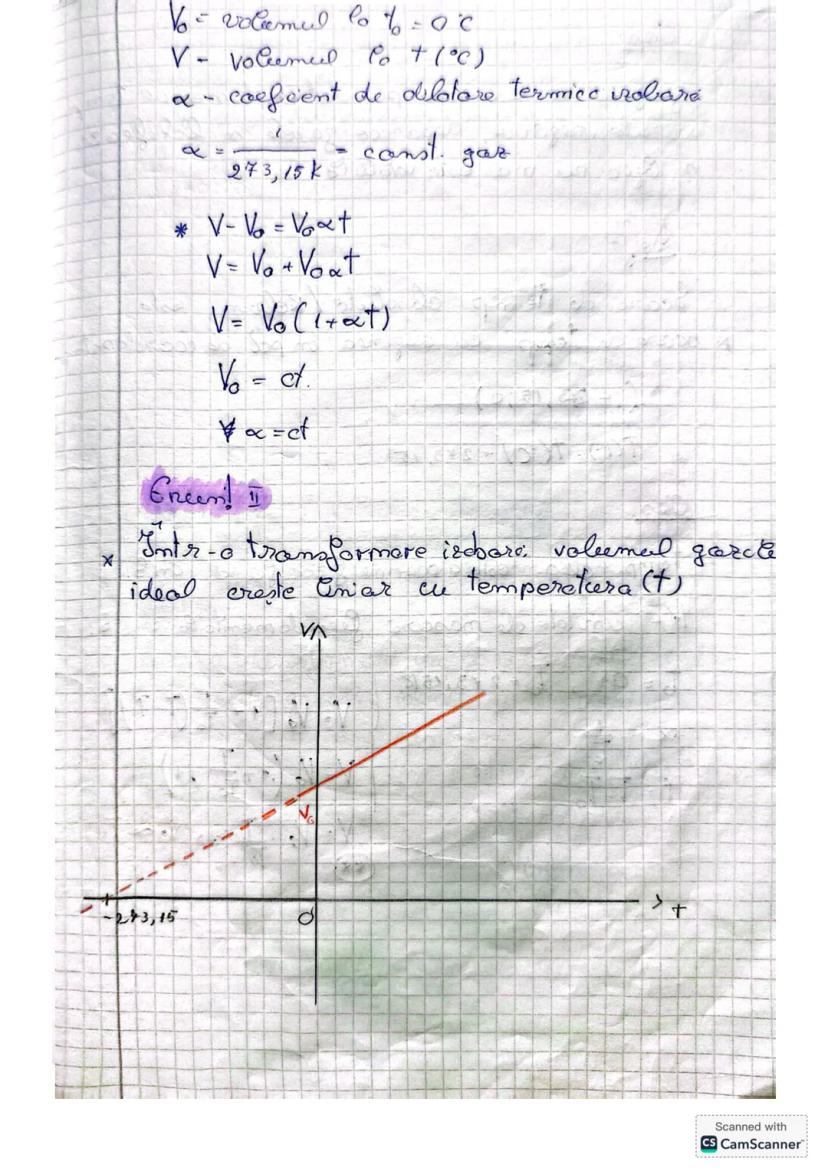
Formulată altfel, legea spune că într-o transformare izobară, volumul gazului crește liniar cu temperatura. Putem scrie: V = V₀, o ecuație care ne arată clar această dependență liniară.
💡 Poți să-ți imaginezi legea Gay-Lussac privind un balon care se mărește când îl încălzești, fără să-i modifici presiunea!
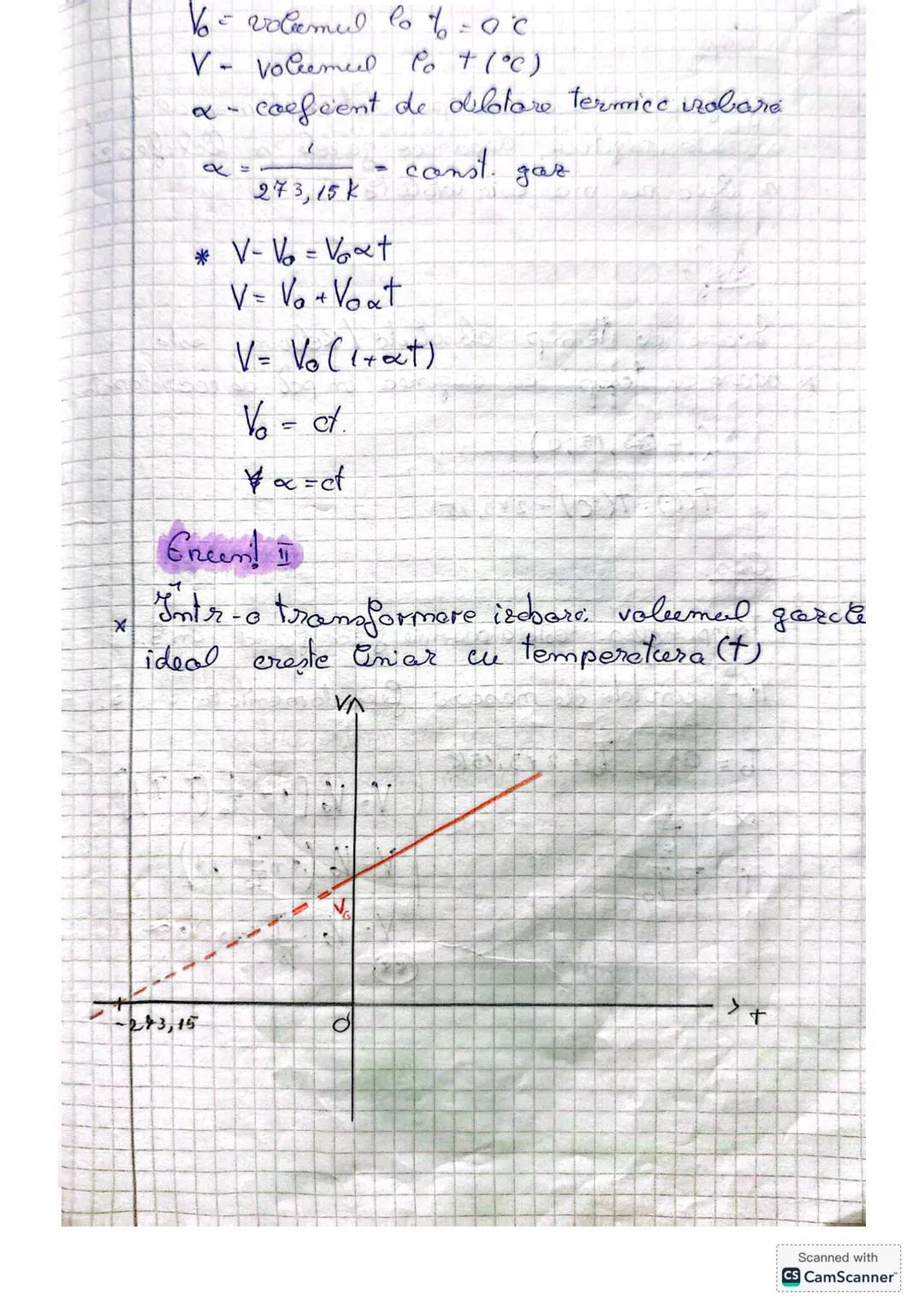
Transformarea izobară (continuare)
Legea Gay-Lussac poate fi reformulată și mai simplu folosind temperatura absolută (în Kelvin). Când lucrăm cu temperatura absolută, relația devine direct proporțională: V = V₀ × T/T₀.
Simplificând ecuația V = V₀, și ținând cont că α = 1/T₀, ajungem la o formulă elegantă: V/T = constant. Această formulă e mult mai ușor de aplicat în probleme.
Graficul unei transformări izobare este o linie dreaptă care pornește din origine când folosim coordonatele V și T. Această reprezentare ne ajută să vizualizăm cum volumul crește odată cu temperatura.
💡 Atenție! Graficele pentru gaze sunt valabile doar pentru domeniul de temperaturi în care substanța rămâne în stare gazoasă - la temperaturi prea joase gazele se lichefiază și legile nu mai sunt aplicabile.

Temperatura absolută (Kelvin)
Scara Kelvin este fundamentală în studiul gazelor ideale. Ea are originea la -273,15°C, punctul numit zero absolut, temperatura teoretică la care un gaz ar avea volum zero (în realitate, gazele se lichefiază înainte de a atinge această temperatură).
Pentru a converti din grade Celsius în Kelvin folosim formula: T(K) = t(°C) + 273,15. De exemplu, 0°C corespunde cu 273,15K.
În Sistemul Internațional, temperatura absolută (T) este o mărime fizică fundamentală, iar Kelvin (K) este unitatea de măsură fundamentală. Folosirea temperaturii absolute simplifică enorm ecuațiile gazelor ideale.
💡 Zero absolut reprezintă temperatura teoretică la care particulele unui gaz ar avea energie cinetică zero - practic imposibil de atins în practică!
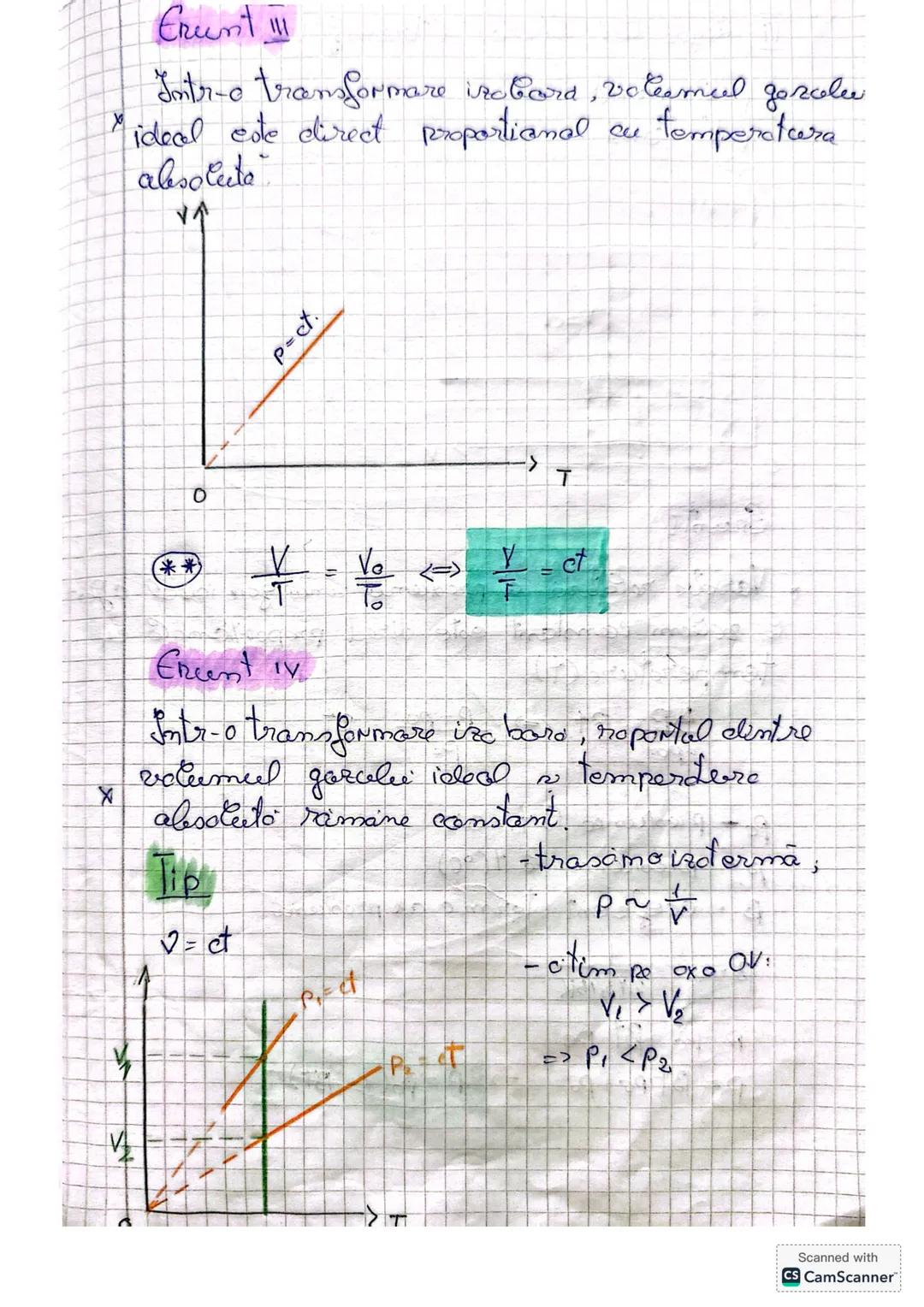
Transformarea izobară (formulări alternative)
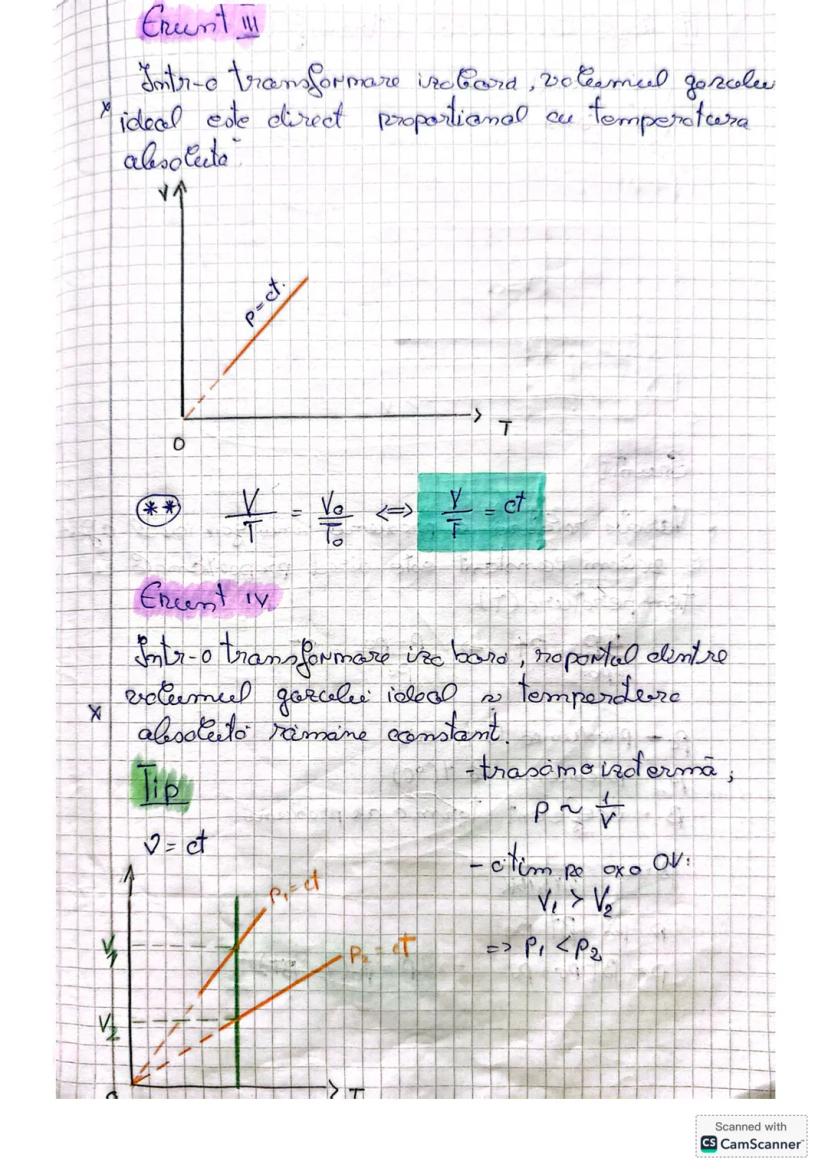
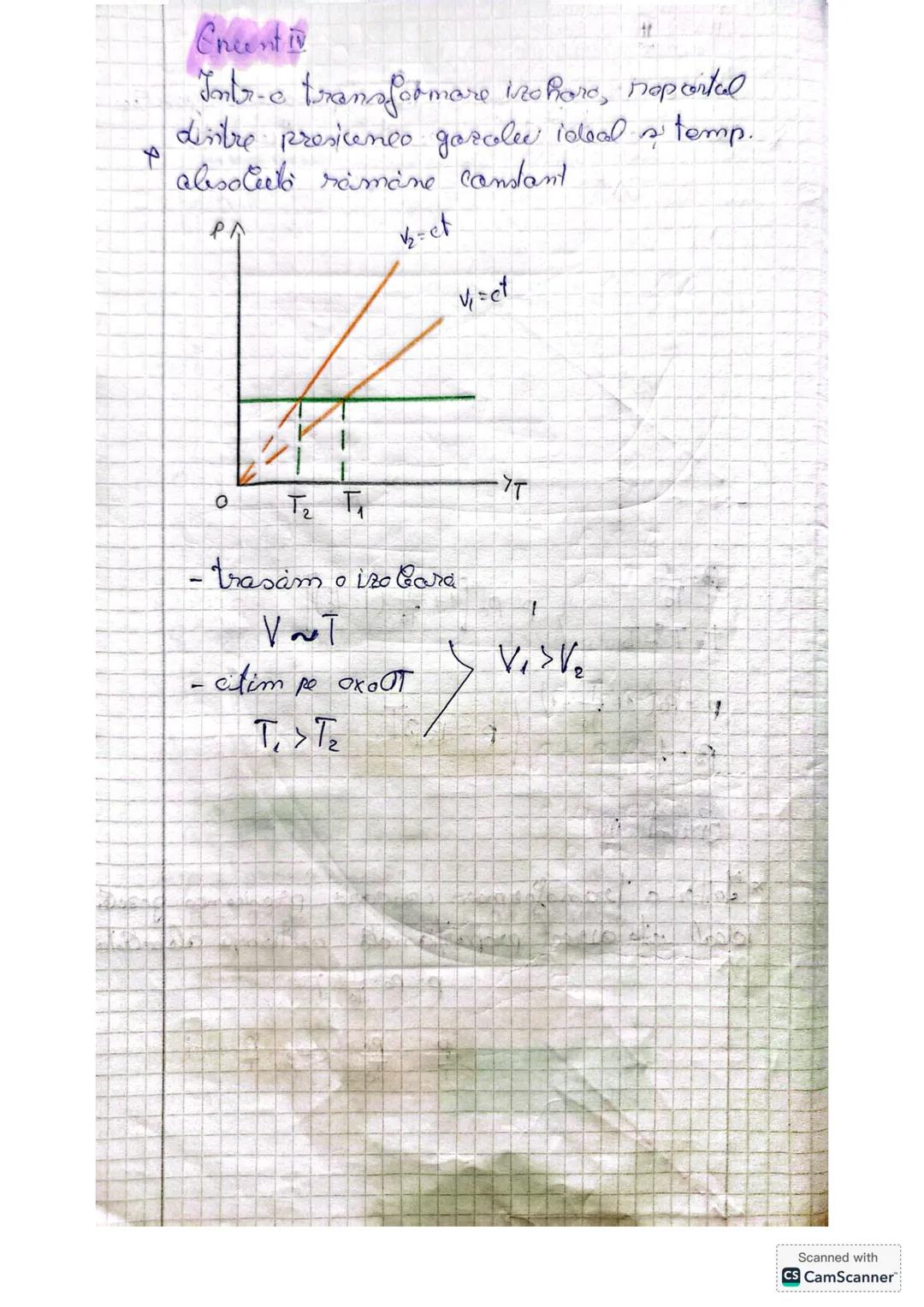
Într-o transformare izobară (la presiune constantă), volumul gazului ideal este direct proporțional cu temperatura absolută. Altfel spus, dacă dublezi temperatura absolută, se dublează și volumul gazului.
Matematic, putem scrie: V/T = V₀/T₀ = constant. Această formulare a legii Gay-Lussac este extrem de utilă în calculele practice cu gaze ideale.
Când rezolvi probleme cu transformări, ține minte că pentru transformările izoterme , presiunea variază invers proporțional cu volumul . Dacă citim pe axa OV a unui grafic și observăm V₁ > V₂, atunci putem deduce imediat că P₁ < P₂.
💡 Proporționalitatea directă dintre volum și temperatura absolută înseamnă că poți estima ușor cum se va comporta un gaz când îl încălzești sau răcești la presiune constantă!

Legea lui Charles (Transformarea izocorică)
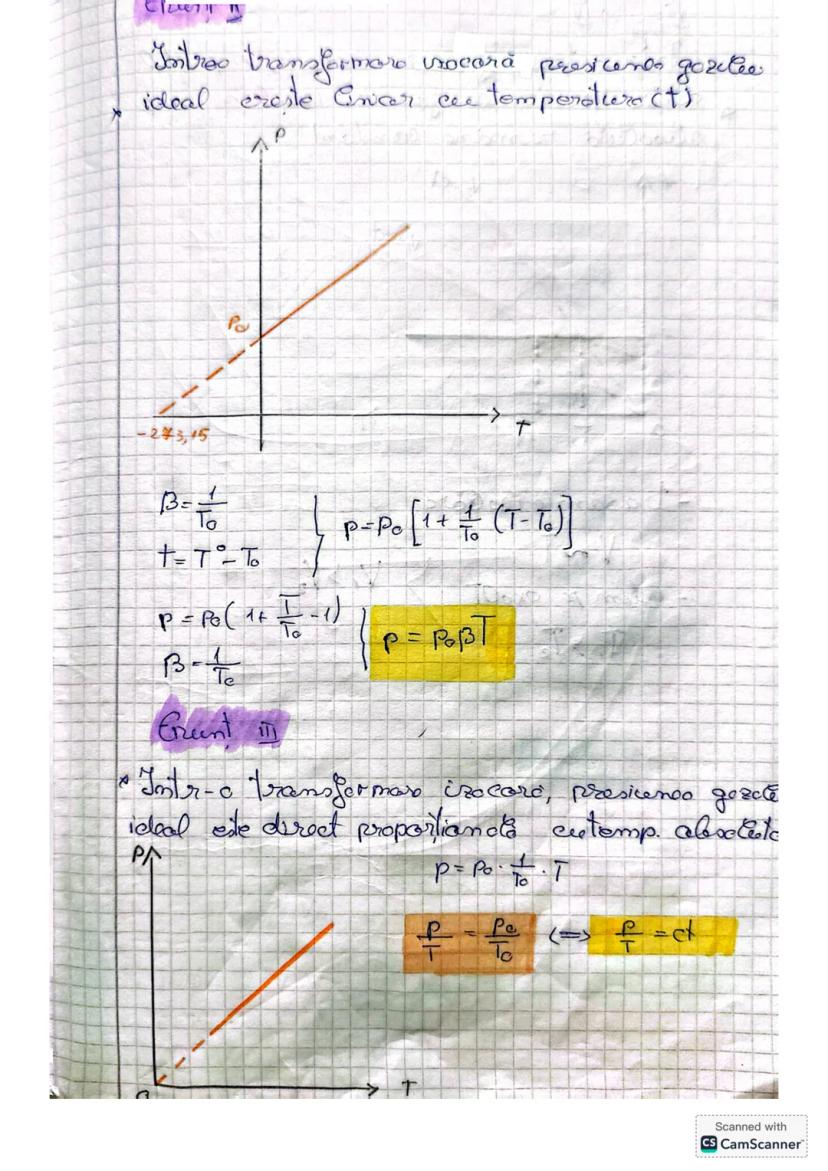
Când volumul rămâne constant, presiunea unui gaz ideal variază direct proporțional cu temperatura. Această transformare, numită izocorică, are aplicații importante în multe procese termice.
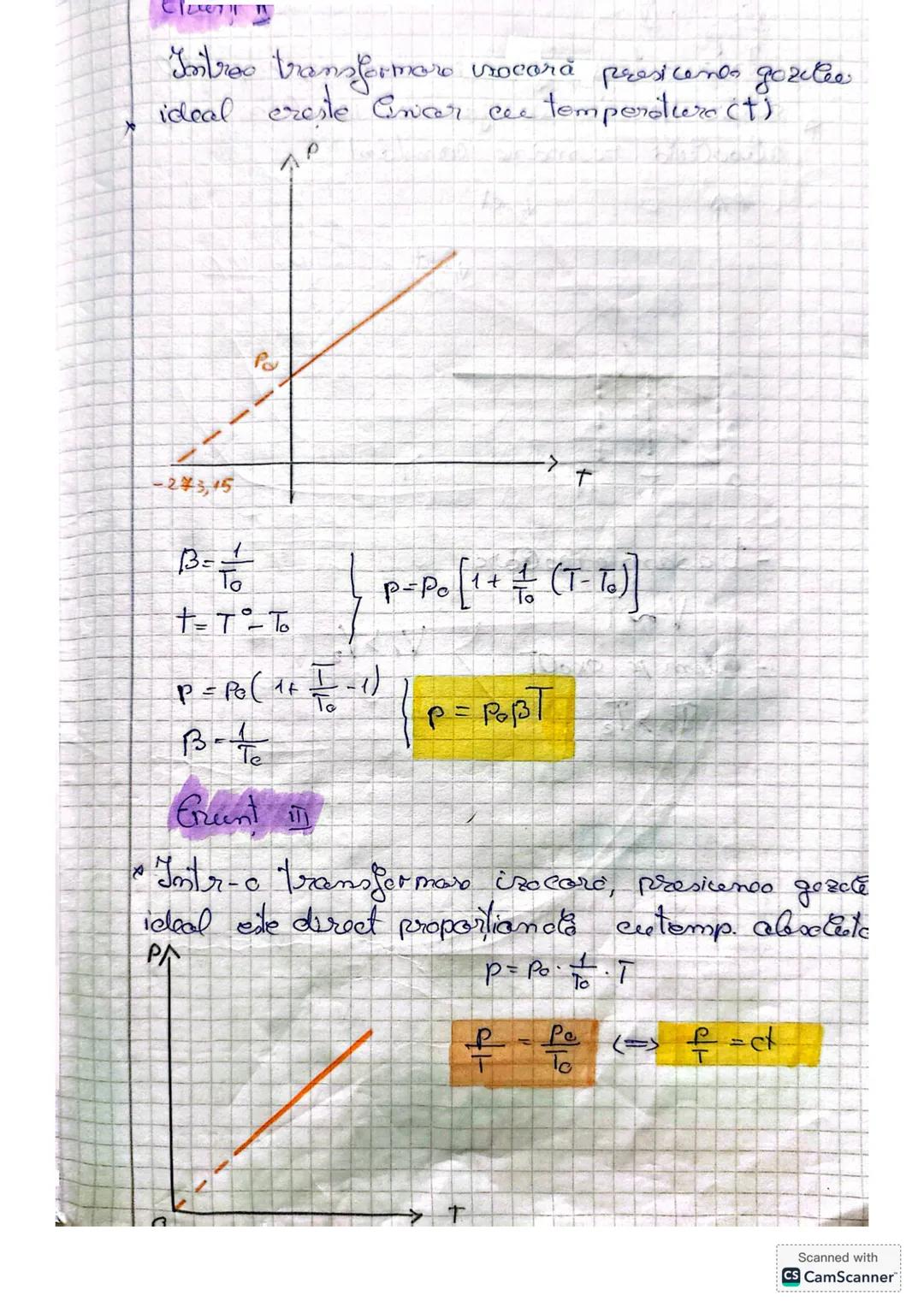
Similar cu legea Gay-Lussac, variația relativă a presiunii este dată de formula: /P₀ = βt, unde P₀ este presiunea la 0°C, iar β este coeficientul termic al presiunii, care are aceeași valoare ca α: β = 1/273,15K.
Transformând ecuația, obținem: P = P₀. Aceasta ne arată că presiunea crește liniar cu temperatura când volumul este menținut constant.
💡 Gândește-te la un recipient închis cu gaz când îl încălzești - presiunea crește pentru că moleculele se mișcă mai repede și lovesc pereții mai des și cu mai multă energie!
Transformarea izocorică (continuare)
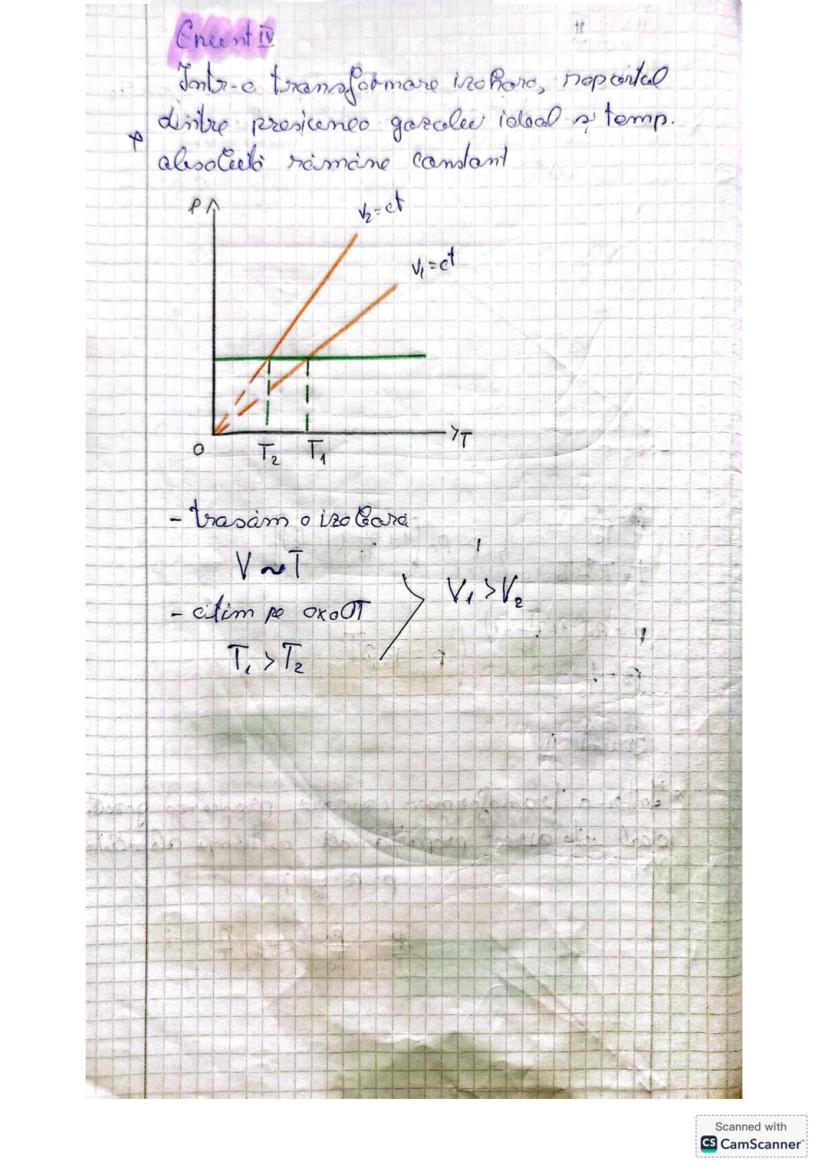
Într-o transformare izocorică, presiunea gazului ideal este direct proporțională cu temperatura absolută. Cu cât temperatura este mai mare, cu atât moleculele gazului se mișcă mai rapid, lovind pereții recipientului cu o forță mai mare.
Folosind temperatura absolută (în Kelvin), putem rescrie legea sub forma simplă: P = P₀ × T/T₀, sau echivalent: P/T = P₀/T₀ = constant.
Graficul unei transformări izocorice este o linie dreaptă care trece prin origine când reprezentăm presiunea în funcție de temperatura absolută. Extinderea acestui grafic la temperaturi negative extreme ar duce teoretic la presiune zero la zero absolut.
💡 Transformările izocorice apar în multe situații practice - de exemplu, când încălzești un recipient complet închis, cum ar fi o conservă expusă la soare!
Ecuația generală a gazelor ideale
Combinând toate transformările studiate anterior, obținem ecuația generală a gazelor ideale: PV/T = constant sau P₁V₁/T₁ = P₂V₂/T₂. Această ecuație este valabilă pentru orice transformare a unui gaz ideal.
Un caz special este ecuația Clapeyron-Mendeleev: PV = νRT, unde ν este numărul de moli, iar R este constanta universală a gazelor. Valoarea lui R este aproximativ 8,31 J/(mol·K).
Această constantă a fost determinată experimental din condițiile normale: la P₀ = 1 atm = 1,013·10⁵ Pa, T₀ = 273,15 K, un mol de gaz ideal ocupă V₀ = 22,4·10⁻³ m³. Calculul ne dă R = P₀V₀/T₀ ≈ 8,31 J/(mol·K).
💡 Ecuația generală a gazelor ideale este una dintre cele mai importante relații din fizică, permițându-ne să analizăm comportamentul gazelor în orice condiții!

Densitatea gazelor ideale
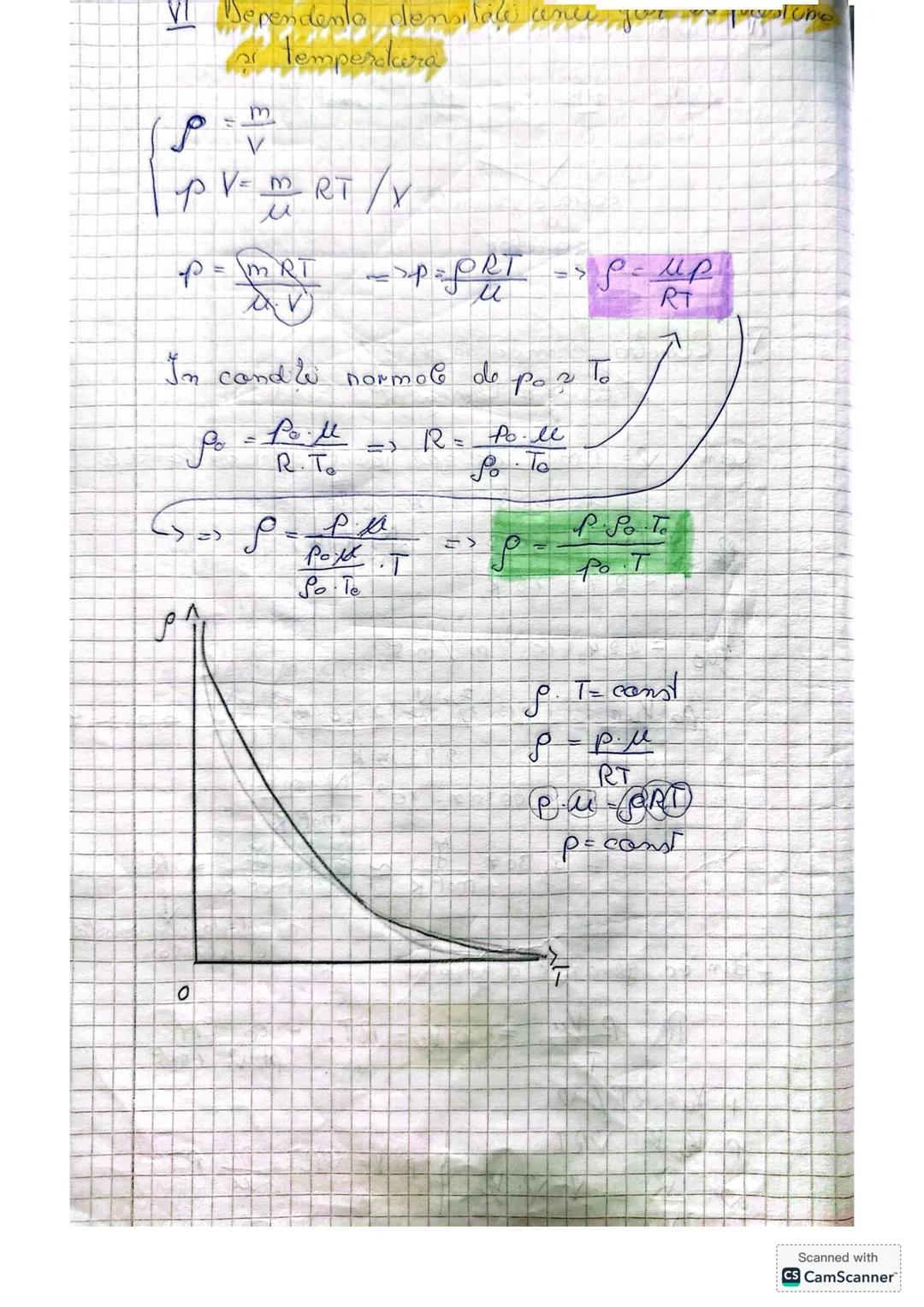
Densitatea unui gaz ideal depinde de presiune, temperatură și masa molară. Pornind de la ecuația Clapeyron-Mendeleev și definiția densității , putem deduce o relație directă:
Ecuația ρ = μP/RT arată că densitatea unui gaz ideal este direct proporțională cu presiunea și invers proporțională cu temperatura absolută. Aici μ reprezintă masa molară a gazului.
În condiții normale (P₀, T₀), densitatea unui gaz depinde doar de masa sa molară: ρ₀ = μP₀/RT₀. Gazele cu mase molare mai mari (precum dioxidul de carbon) au densități mai mari decât cele cu mase molare mici (precum hidrogenul).
💡 Această dependență de temperatură explică de ce aerul cald se ridică - la temperatură mai mare, densitatea scade, făcând gazul mai ușor decât aerul înconjurător!
Aplicații practice și observații importante
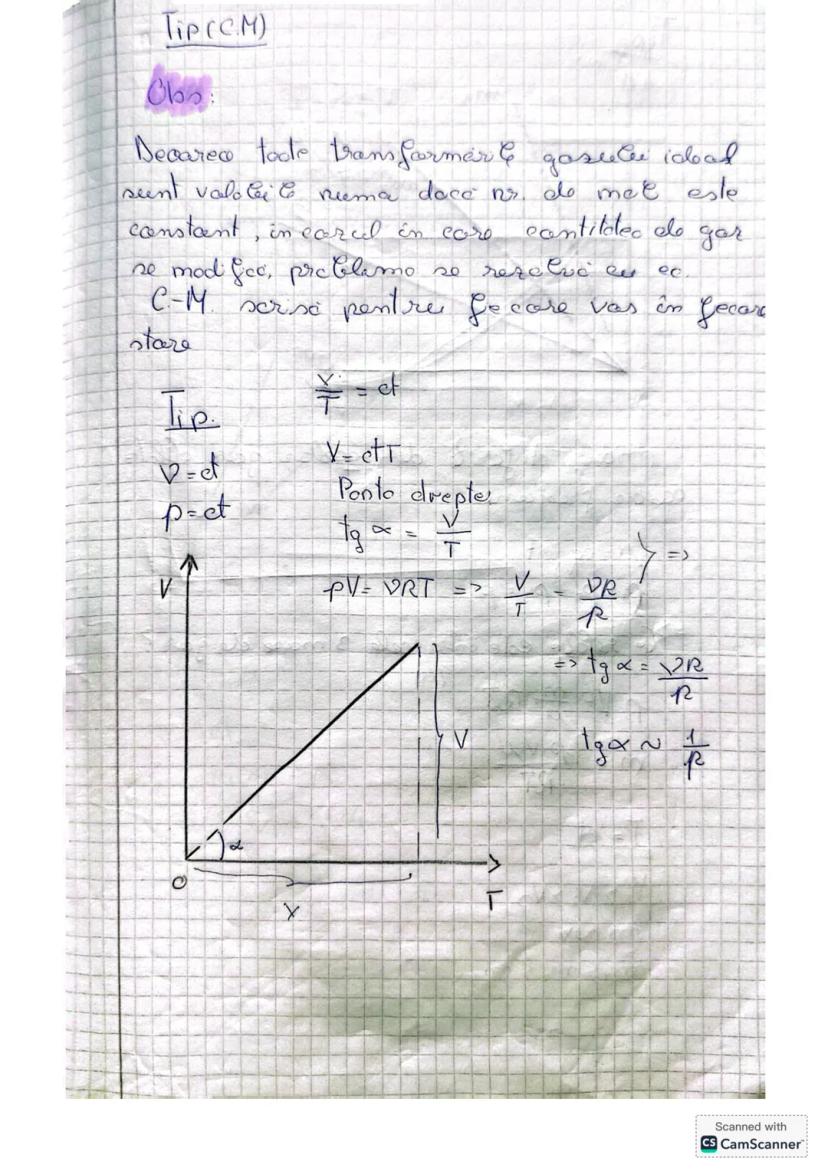
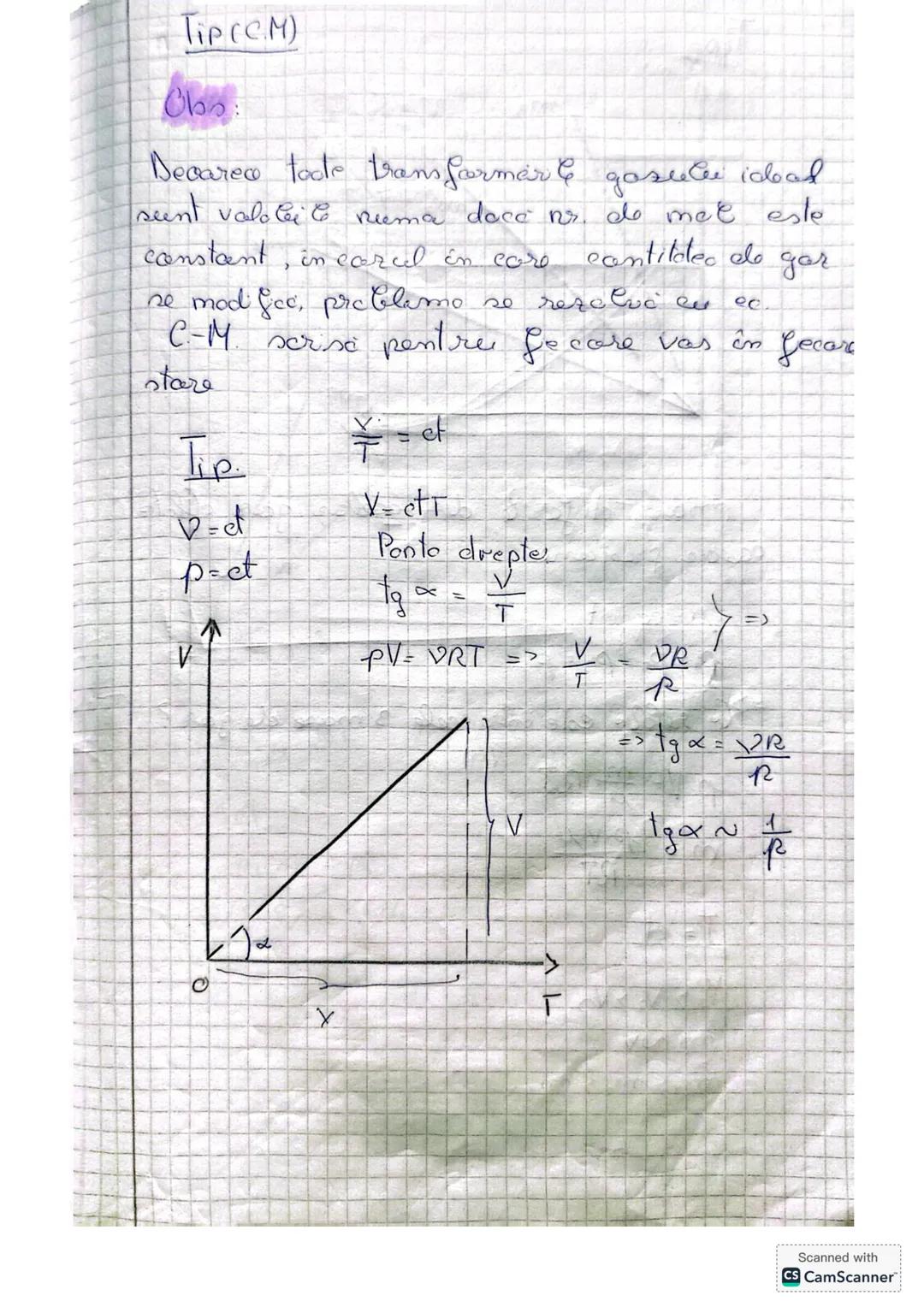
Toate legile gazelor ideale sunt valabile doar când numărul de moli rămâne constant. Când cantitatea de gaz se modifică, trebuie să aplicăm ecuația Clapeyron-Mendeleev pentru fiecare stare în parte.
În transformarea izobară, panta dreptei din graficul V-T este legată de numărul de moli: tg α = V/T = νR/P. Astfel, cu cât avem mai mult gaz, cu atât panta este mai mare.
Pentru a rezolva eficient probleme cu gaze, identifică mai întâi tipul transformării (izotermă, izobară, izocorică sau generală), apoi alege formula potrivită:
- Izotermă: PV = constant
- Izobară: V/T = constant
- Izocorică: P/T = constant
- Generală: PV/T = constant
💡 Reține că toate aceste legi sunt idealizări - gazele reale urmează aceste legi cu precizie doar la presiuni scăzute și temperaturi ridicate, când interacțiunile dintre molecule sunt neglijabile!
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut la Matematică
9EN CLASA a6
Evaluarea națională pentru clasa a-6-a matematica fizica și biologie
Formule Mecanica BAC
Formule pentru BAC la Fizica - Mecanica
Fizica Electricitate
formule cu mici explicatii
Materie optica-admitere medicina
Toata materia necesara pt capitolul de optica✨
Termodinamica-materie admitere medicina
Tot capitolul de termodinamica pentru admiterea la medicina!✨
MECANICA
PROGRAMA DE BACALAUREAT PENTRU MECANICA
Materie electricitate-admitere medicina
Toata materia de la capitolul de electricitate pentru admitere la facultatea de medicina✨
Electricitate -Teoremele lui Kirchhoff
Teoremele lui Kirchhoff
Evaluarea Națională 2024-2025
clasa a 6-a
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Legile Gazului în Termodinamică
Legile gazelor ideale sunt fundamentul termodinamicii și explică comportamentul gazelor în diverse condiții. Aceste legi descriu relațiile matematice între presiune, volum și temperatură, permițându-ne să prezicem cum se va comporta un gaz când unul dintre acești parametri se modifică.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Legea Boyle-Mariotte (Transformarea izotermă)
La temperatura constantă, presiunea unui gaz ideal variază invers proporțional cu volumul său. Adică, dacă volumul scade, presiunea crește și invers.
Formula matematică a acestei legi este foarte simplă: p·V = constant. Această ecuație descrie o izotermă, care grafic apare ca o hiperbolă.
Pe grafic, putem observa cum la volume mari presiunea este mică, iar când volumul scade, presiunea crește brusc. E ca atunci când comprimi aerul într-o pompă de bicicletă - simți cum devine din ce în ce mai greu să împingi!
💡 Când rezolvi probleme cu transformări izoterme, amintește-ți că produsul p·V rămâne același în orice punct al transformării.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Legea Gay-Lussac (Transformarea izobară)
La presiune constantă, volumul unui gaz ideal variază direct proporțional cu temperatura. Când încălzești un gaz menținând presiunea constantă, acesta se dilată uniform.
Matematic, variația relativă a volumului se exprimă prin formula: /V₀ = α × t, unde V₀ este volumul la 0°C, iar α este coeficientul de dilatare termică volumară al gazului, egal cu aproximativ 1/273,15 K⁻¹.
Formulată altfel, legea spune că într-o transformare izobară, volumul gazului crește liniar cu temperatura. Putem scrie: V = V₀, o ecuație care ne arată clar această dependență liniară.
💡 Poți să-ți imaginezi legea Gay-Lussac privind un balon care se mărește când îl încălzești, fără să-i modifici presiunea!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Transformarea izobară (continuare)
Legea Gay-Lussac poate fi reformulată și mai simplu folosind temperatura absolută (în Kelvin). Când lucrăm cu temperatura absolută, relația devine direct proporțională: V = V₀ × T/T₀.
Simplificând ecuația V = V₀, și ținând cont că α = 1/T₀, ajungem la o formulă elegantă: V/T = constant. Această formulă e mult mai ușor de aplicat în probleme.
Graficul unei transformări izobare este o linie dreaptă care pornește din origine când folosim coordonatele V și T. Această reprezentare ne ajută să vizualizăm cum volumul crește odată cu temperatura.
💡 Atenție! Graficele pentru gaze sunt valabile doar pentru domeniul de temperaturi în care substanța rămâne în stare gazoasă - la temperaturi prea joase gazele se lichefiază și legile nu mai sunt aplicabile.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Temperatura absolută (Kelvin)
Scara Kelvin este fundamentală în studiul gazelor ideale. Ea are originea la -273,15°C, punctul numit zero absolut, temperatura teoretică la care un gaz ar avea volum zero (în realitate, gazele se lichefiază înainte de a atinge această temperatură).
Pentru a converti din grade Celsius în Kelvin folosim formula: T(K) = t(°C) + 273,15. De exemplu, 0°C corespunde cu 273,15K.
În Sistemul Internațional, temperatura absolută (T) este o mărime fizică fundamentală, iar Kelvin (K) este unitatea de măsură fundamentală. Folosirea temperaturii absolute simplifică enorm ecuațiile gazelor ideale.
💡 Zero absolut reprezintă temperatura teoretică la care particulele unui gaz ar avea energie cinetică zero - practic imposibil de atins în practică!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Transformarea izobară (formulări alternative)
Într-o transformare izobară (la presiune constantă), volumul gazului ideal este direct proporțional cu temperatura absolută. Altfel spus, dacă dublezi temperatura absolută, se dublează și volumul gazului.
Matematic, putem scrie: V/T = V₀/T₀ = constant. Această formulare a legii Gay-Lussac este extrem de utilă în calculele practice cu gaze ideale.
Când rezolvi probleme cu transformări, ține minte că pentru transformările izoterme , presiunea variază invers proporțional cu volumul . Dacă citim pe axa OV a unui grafic și observăm V₁ > V₂, atunci putem deduce imediat că P₁ < P₂.
💡 Proporționalitatea directă dintre volum și temperatura absolută înseamnă că poți estima ușor cum se va comporta un gaz când îl încălzești sau răcești la presiune constantă!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Legea lui Charles (Transformarea izocorică)
Când volumul rămâne constant, presiunea unui gaz ideal variază direct proporțional cu temperatura. Această transformare, numită izocorică, are aplicații importante în multe procese termice.
Similar cu legea Gay-Lussac, variația relativă a presiunii este dată de formula: /P₀ = βt, unde P₀ este presiunea la 0°C, iar β este coeficientul termic al presiunii, care are aceeași valoare ca α: β = 1/273,15K.
Transformând ecuația, obținem: P = P₀. Aceasta ne arată că presiunea crește liniar cu temperatura când volumul este menținut constant.
💡 Gândește-te la un recipient închis cu gaz când îl încălzești - presiunea crește pentru că moleculele se mișcă mai repede și lovesc pereții mai des și cu mai multă energie!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Transformarea izocorică (continuare)
Într-o transformare izocorică, presiunea gazului ideal este direct proporțională cu temperatura absolută. Cu cât temperatura este mai mare, cu atât moleculele gazului se mișcă mai rapid, lovind pereții recipientului cu o forță mai mare.
Folosind temperatura absolută (în Kelvin), putem rescrie legea sub forma simplă: P = P₀ × T/T₀, sau echivalent: P/T = P₀/T₀ = constant.
Graficul unei transformări izocorice este o linie dreaptă care trece prin origine când reprezentăm presiunea în funcție de temperatura absolută. Extinderea acestui grafic la temperaturi negative extreme ar duce teoretic la presiune zero la zero absolut.
💡 Transformările izocorice apar în multe situații practice - de exemplu, când încălzești un recipient complet închis, cum ar fi o conservă expusă la soare!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Ecuația generală a gazelor ideale
Combinând toate transformările studiate anterior, obținem ecuația generală a gazelor ideale: PV/T = constant sau P₁V₁/T₁ = P₂V₂/T₂. Această ecuație este valabilă pentru orice transformare a unui gaz ideal.
Un caz special este ecuația Clapeyron-Mendeleev: PV = νRT, unde ν este numărul de moli, iar R este constanta universală a gazelor. Valoarea lui R este aproximativ 8,31 J/(mol·K).
Această constantă a fost determinată experimental din condițiile normale: la P₀ = 1 atm = 1,013·10⁵ Pa, T₀ = 273,15 K, un mol de gaz ideal ocupă V₀ = 22,4·10⁻³ m³. Calculul ne dă R = P₀V₀/T₀ ≈ 8,31 J/(mol·K).
💡 Ecuația generală a gazelor ideale este una dintre cele mai importante relații din fizică, permițându-ne să analizăm comportamentul gazelor în orice condiții!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Densitatea gazelor ideale
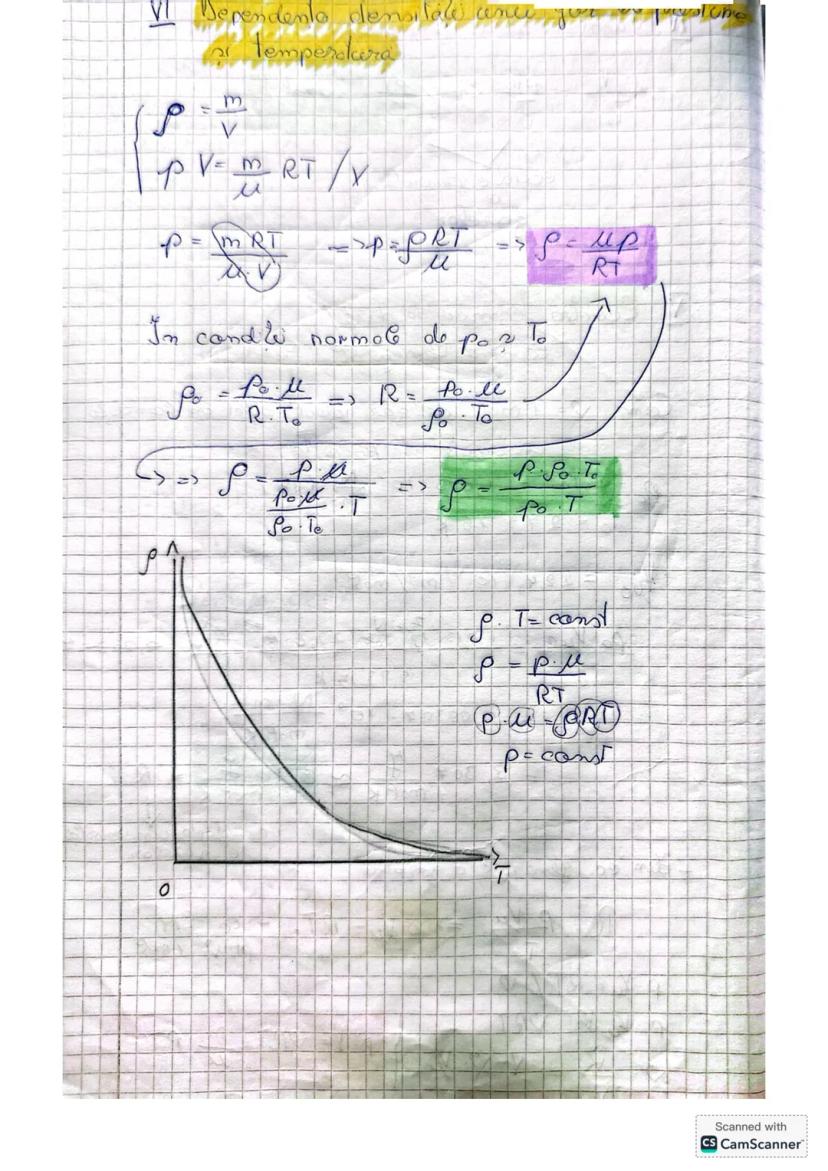
Densitatea unui gaz ideal depinde de presiune, temperatură și masa molară. Pornind de la ecuația Clapeyron-Mendeleev și definiția densității , putem deduce o relație directă:
Ecuația ρ = μP/RT arată că densitatea unui gaz ideal este direct proporțională cu presiunea și invers proporțională cu temperatura absolută. Aici μ reprezintă masa molară a gazului.
În condiții normale (P₀, T₀), densitatea unui gaz depinde doar de masa sa molară: ρ₀ = μP₀/RT₀. Gazele cu mase molare mai mari (precum dioxidul de carbon) au densități mai mari decât cele cu mase molare mici (precum hidrogenul).
💡 Această dependență de temperatură explică de ce aerul cald se ridică - la temperatură mai mare, densitatea scade, făcând gazul mai ușor decât aerul înconjurător!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Aplicații practice și observații importante
Toate legile gazelor ideale sunt valabile doar când numărul de moli rămâne constant. Când cantitatea de gaz se modifică, trebuie să aplicăm ecuația Clapeyron-Mendeleev pentru fiecare stare în parte.
În transformarea izobară, panta dreptei din graficul V-T este legată de numărul de moli: tg α = V/T = νR/P. Astfel, cu cât avem mai mult gaz, cu atât panta este mai mare.
Pentru a rezolva eficient probleme cu gaze, identifică mai întâi tipul transformării (izotermă, izobară, izocorică sau generală), apoi alege formula potrivită:
- Izotermă: PV = constant
- Izobară: V/T = constant
- Izocorică: P/T = constant
- Generală: PV/T = constant
💡 Reține că toate aceste legi sunt idealizări - gazele reale urmează aceste legi cu precizie doar la presiuni scăzute și temperaturi ridicate, când interacțiunile dintre molecule sunt neglijabile!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut la Matematică
9EN CLASA a6
Evaluarea națională pentru clasa a-6-a matematica fizica și biologie
Formule Mecanica BAC
Formule pentru BAC la Fizica - Mecanica
Fizica Electricitate
formule cu mici explicatii
Materie optica-admitere medicina
Toata materia necesara pt capitolul de optica✨
Termodinamica-materie admitere medicina
Tot capitolul de termodinamica pentru admiterea la medicina!✨
MECANICA
PROGRAMA DE BACALAUREAT PENTRU MECANICA
Materie electricitate-admitere medicina
Toata materia de la capitolul de electricitate pentru admitere la facultatea de medicina✨
Electricitate -Teoremele lui Kirchhoff
Teoremele lui Kirchhoff
Evaluarea Națională 2024-2025
clasa a 6-a
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.