Descoperă cum evoluează proprietățile chimice în tabelul periodic! Vom explora... Afișează mai mult
Proprietățile Elementelor Chimice în Tabelul Periodic






Variația proprietăților elementelor chimice în tabelul periodic
Tabelul periodic nu este doar o simplă listă de elemente, ci un sistem organizat care ne arată cum se schimbă proprietățile elementelor în mod regulat. Aceste schimbări nu sunt întâmplătoare!
Vom vedea cum caracteristicile atomilor variază pe măsură ce ne deplasăm prin perioade (rânduri) și grupe (coloane) în tabel, făcând chimia mult mai ușor de înțeles și de prezis.
Bine de știut: Înțelegerea modului în care variază proprietățile elementelor în tabelul periodic te va ajuta să prezici comportamentul lor chimic fără să memorezi informații pentru fiecare element în parte!
Proprietățile elementelor chimice
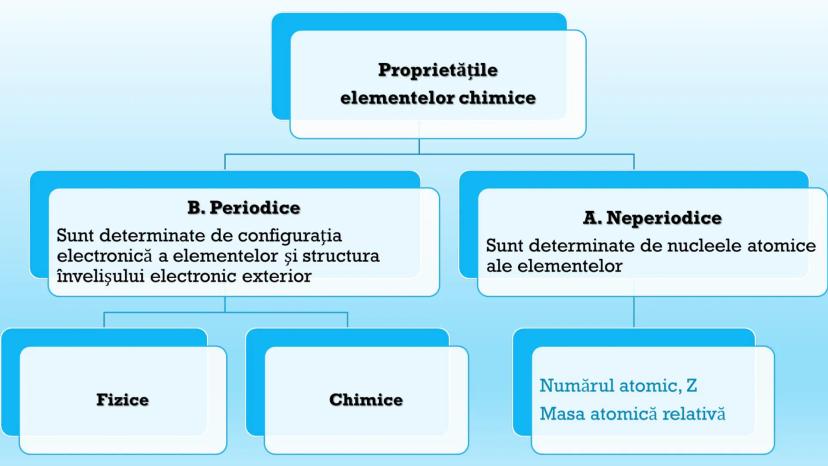
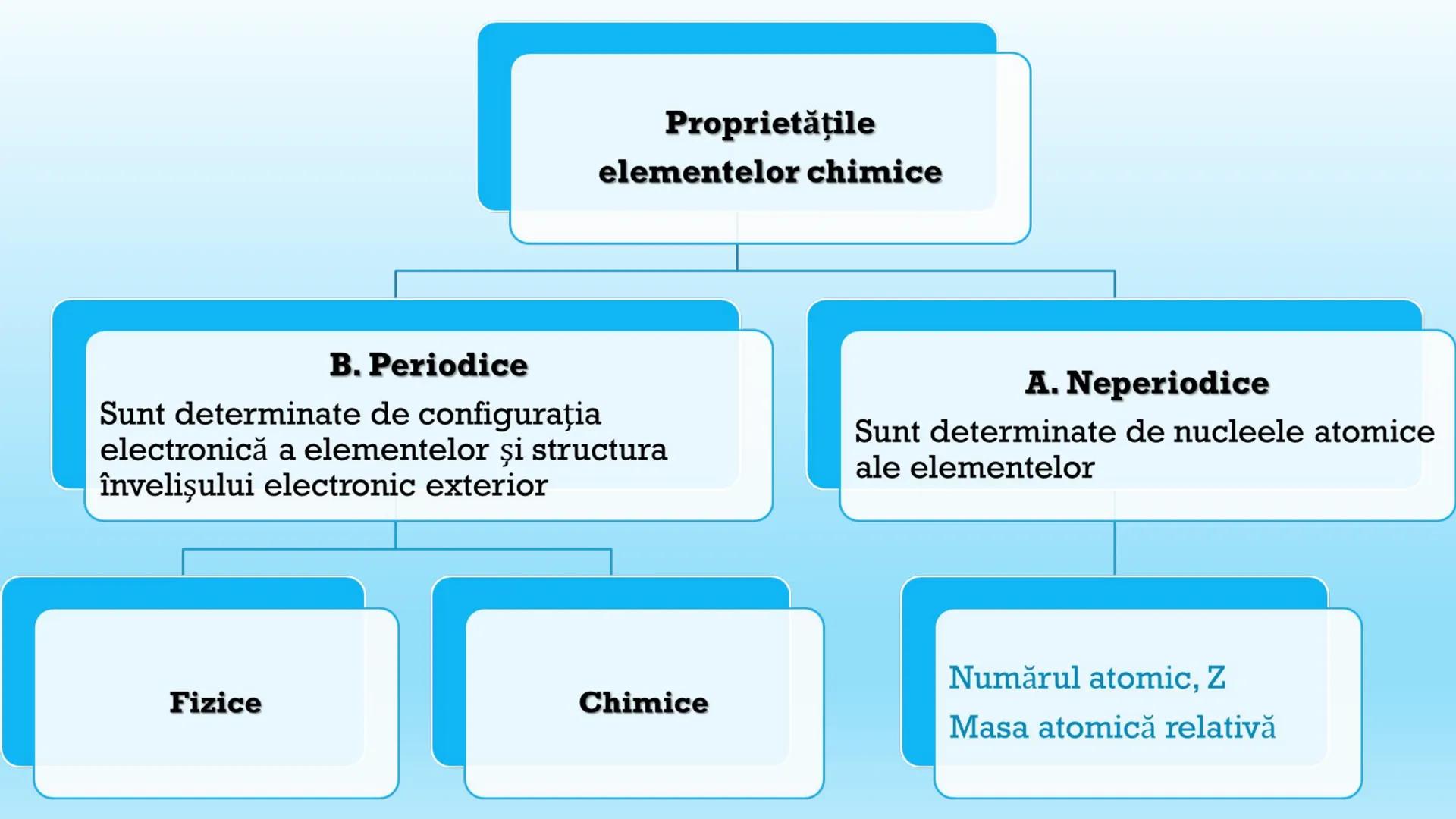
Elementele chimice au două tipuri principale de proprietăți: periodice și neperiodice. Trebuie să le cunoaștem pe ambele pentru a înțelege comportamentul lor!
Proprietățile periodice sunt determinate de configurația electronică și structura învelișului electronic exterior. Acestea variază în mod regulat în tabelul periodic și includ raza atomică, energia de ionizare sau afinitatea pentru electroni.
Proprietățile neperiodice sunt determinate de nucleele atomice și nu urmează un model repetitiv. Cele mai importante sunt numărul atomic (Z) și masa atomică relativă (A), care cresc în general de la un element la altul.
Atenție: Proprietățile periodice sunt cele care ne ajută cel mai mult să înțelegem și să prezicem reactivitatea chimică a elementelor!

Numărul atomic și masa atomică
Numărul atomic (Z) reprezintă proprietatea fundamentală a atomilor și crește cu câte o unitate de la un element la altul în tabelul periodic. Acesta ne arată numărul de protoni din nucleu și determină identitatea elementului.
Masa atomică relativă (A) crește de la primul element până la ultimul din sistem. Inițial, oamenii de știință credeau că masa atomică este proprietatea fundamentală a elementelor.
Mai târziu, s-a descoperit că masa atomică este de fapt o proprietate derivată, care depinde de compoziția izotopică a fiecărui element - adică de amestecul de izotopi cu diferite numere de neutroni.
Interesant: Deși masa atomică crește în general în tabelul periodic, există câteva excepții unde elementul cu Z mai mare are masă atomică mai mică!
Proprietăți fizice periodice
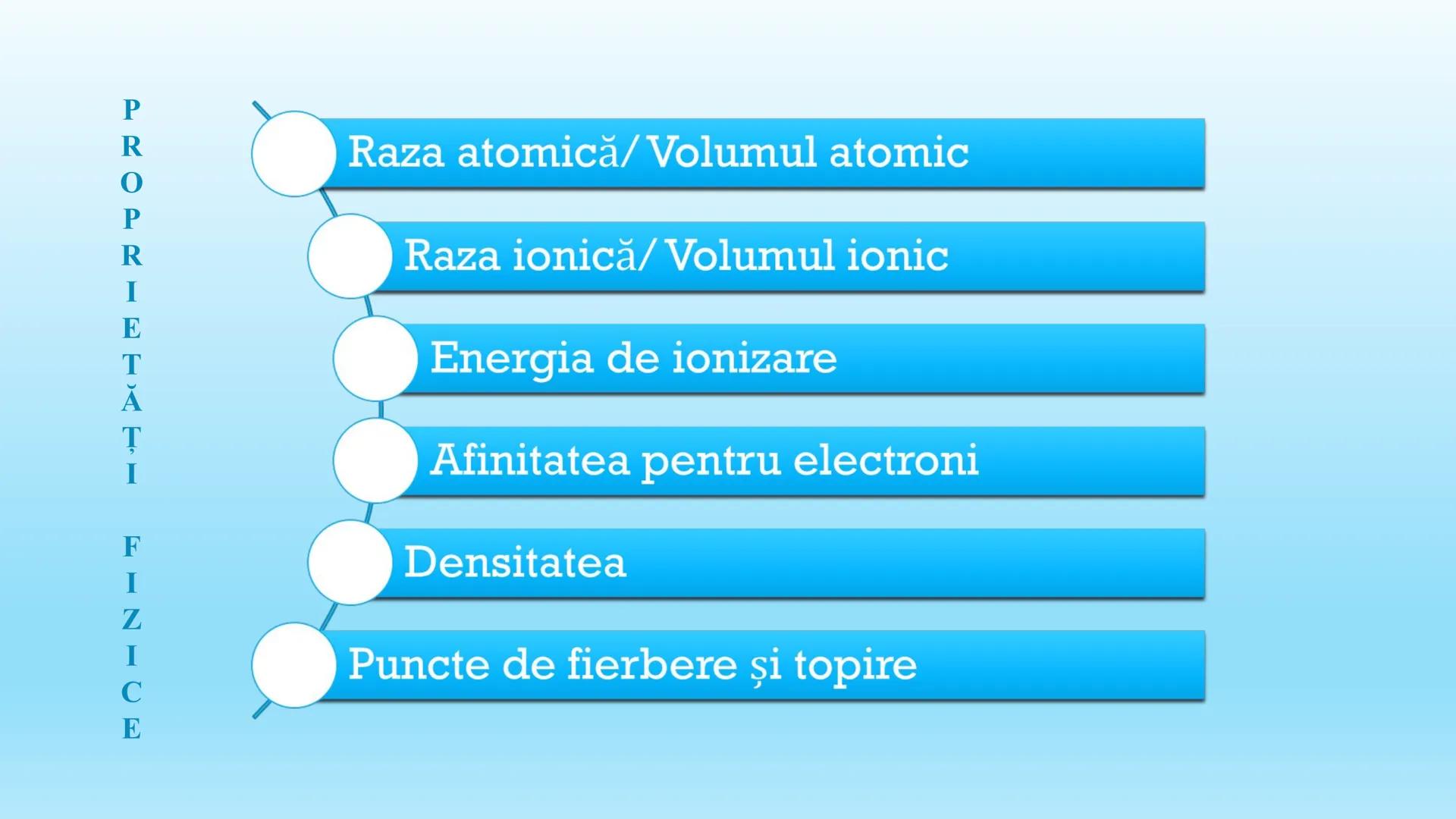
Când explorăm tabelul periodic, putem observa că multe proprietăți fizice se schimbă în mod regulat. Acestea ne ajută să înțelegem comportamentul elementelor!
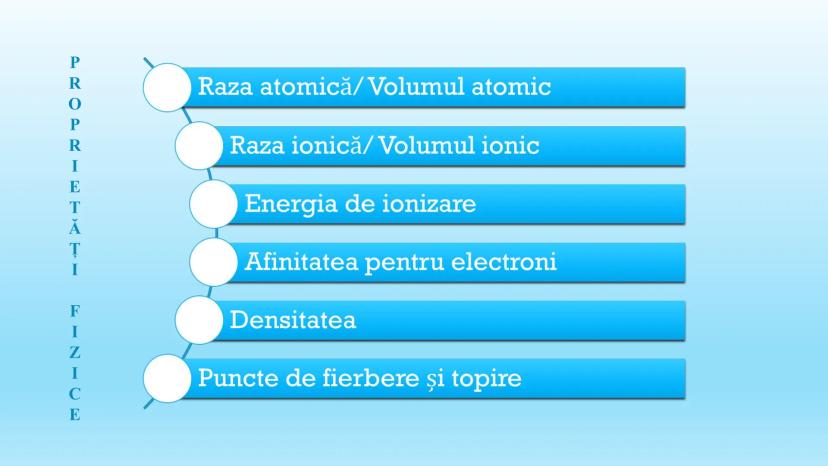
Printre cele mai importante proprietăți fizice periodice se numără raza atomică și volumul atomic, care ne arată dimensiunea atomilor. De asemenea, avem raza ionică și volumul ionic pentru atomi care au câștigat sau pierdut electroni.
Alte proprietăți esențiale includ energia de ionizare (energia necesară pentru a îndepărta un electron), afinitatea pentru electroni (tendința de a atrage electroni), densitatea și punctele de fierbere și topire.
Aplicație practică: Aceste proprietăți ne ajută să înțelegem de ce unele metale sunt moi (ca sodiul), iar altele sunt dure (ca titanul), sau de ce unele elemente sunt gaze la temperatura camerei, iar altele sunt solide.

Raza atomică
Raza atomică este un concept important, deși în realitate atomii nu au o limită clară ca o bilă solidă. Dimensiunile atomilor se calculează folosind mecanica cuantică și depind de starea în care se află atomul.
Un atom poate avea dimensiuni diferite dacă este izolat (rază atomică) sau legat de alți atomi în molecule (rază covalentă) sau în rețele cristaline (rază metalică sau rază ionică). Aceste diferențe sunt esențiale pentru a înțelege comportamentul chimic al elementelor.
În viziunea mecanicii cuantice, norul electronic al atomului este difuz, fără o limită clară. Totuși, pentru explicarea proprietăților, considerăm raza atomului liber ca fiind distanța de la nucleu până la punctul unde densitatea electronilor este maximă.
Ușor de reținut: Gândește-te la atom ca la un nor difuz de electroni în jurul nucleului, nu ca la o sferă solidă cu margini precise. Raza atomică este doar o convenție utilă!
Raze atomice
Raza atomică se poate măsura în diferite moduri, în funcție de contextul în care se află atomul. Este important să înțelegem aceste diferențe!
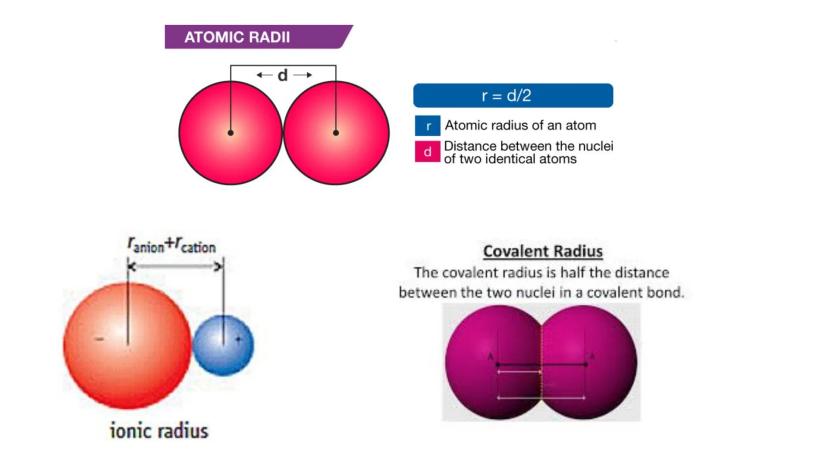
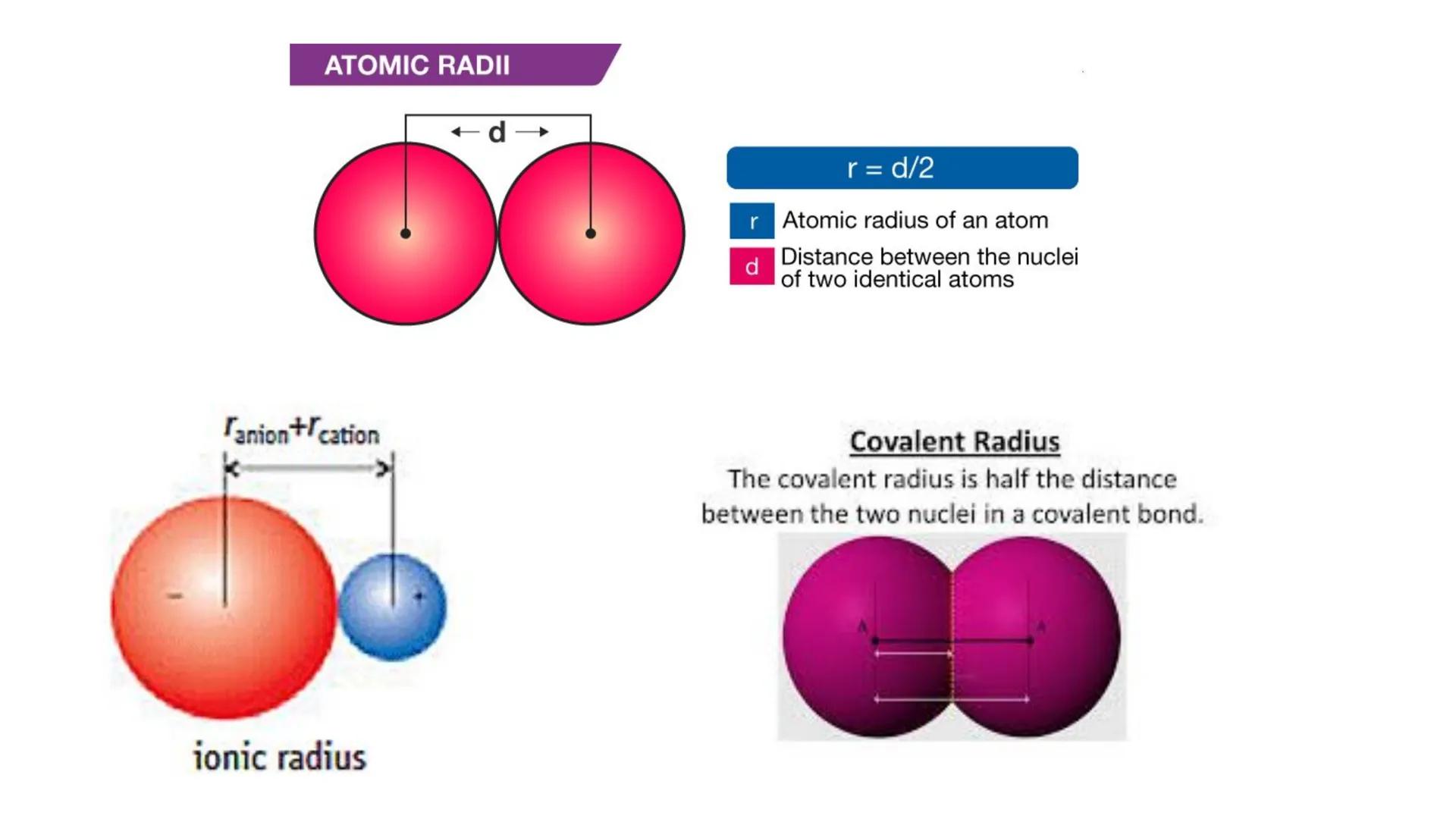
Pentru atomii identici legați între ei, raza atomică (r) se definește ca jumătate din distanța (d) dintre nucleele celor doi atomi: r = d/2. Această măsurătoare ne ajută să înțelegem dimensiunea reală a atomilor.
În cazul compușilor ionici, măsurăm suma razelor ionice: raza anionului + raza cationului. Aceasta ne arată distanța dintre nucleele ionilor vecini cu sarcini opuse.
Pentru legăturile covalente, folosim raza covalentă, care reprezintă jumătate din distanța dintre nucleele a doi atomi identici uniți printr-o legătură covalentă.
Aplicație: Când doi atomi diferit formează o legătură, putem aproxima lungimea legăturii adunând razele lor covalente!

Variația razei atomice
Raza atomică se definește practic ca jumătatea distanței dintre nucleele a doi atomi identici vecini din compuși care conțin atomi, nu ioni. Aceasta se determină prin metode cristalografice precise, folosind difracția cu raze X.
Cum variază raza atomică în cadrul unei grupe din tabelul periodic?
- În grupele principale (elementele s și p), razele atomice cresc semnificativ pe măsură ce coborâm în grupă și crește numărul atomic Z
- În grupele secundare (elementele d), razele atomice cresc doar ușor cu Z, existând o diferență mică între elementele din perioadele 5 și 6
Vizualizează: Imaginează-ți că în fiecare grupă, atomii devin ca niște baloane care se umflă treptat pe măsură ce coborâm în tabel, dar elementele tranziţionale se umflă mult mai puțin!

Variația razei atomice în perioade
Pe măsură ce ne deplasăm de la stânga la dreapta într-o perioadă a tabelului periodic, raza atomică variază în moduri interesante care ne ajută să înțelegem proprietățile elementelor.
În blocul elementelor s și p (grupele principale), razele atomice scad cu creșterea numărului atomic Z. Acest lucru se întâmplă deoarece, deși adăugăm și protoni și electroni, atracția nucleului devine mai puternică și "strânge" norul electronic.
În blocul elementelor d (metalele tranziționale), razele scad de la grupa a 3-a până la grupele 8-10, apoi cresc ușor la elementele din grupele 11-12.
În blocul elementelor f (lantanide și actinide) se observă o scădere ușoară a razelor atomice cu creșterea lui Z, fenomen numit "contracția lantanidelor".
Trucul meu: Pentru a reține tendința generală, gândește-te că în fiecare perioadă, atomii devin tot mai "strânși" pe măsură ce ne deplasăm spre dreapta, până ajungem la gazele nobile.
Tabel periodic și variația razei atomice
În tabelul periodic putem observa modele clare de variație a dimensiunii atomilor, care ne ajută să înțelegem și să prezicem proprietățile chimice.
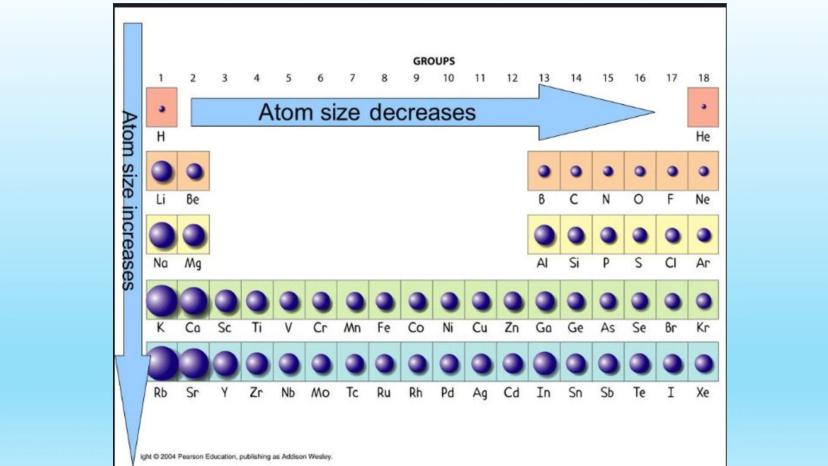
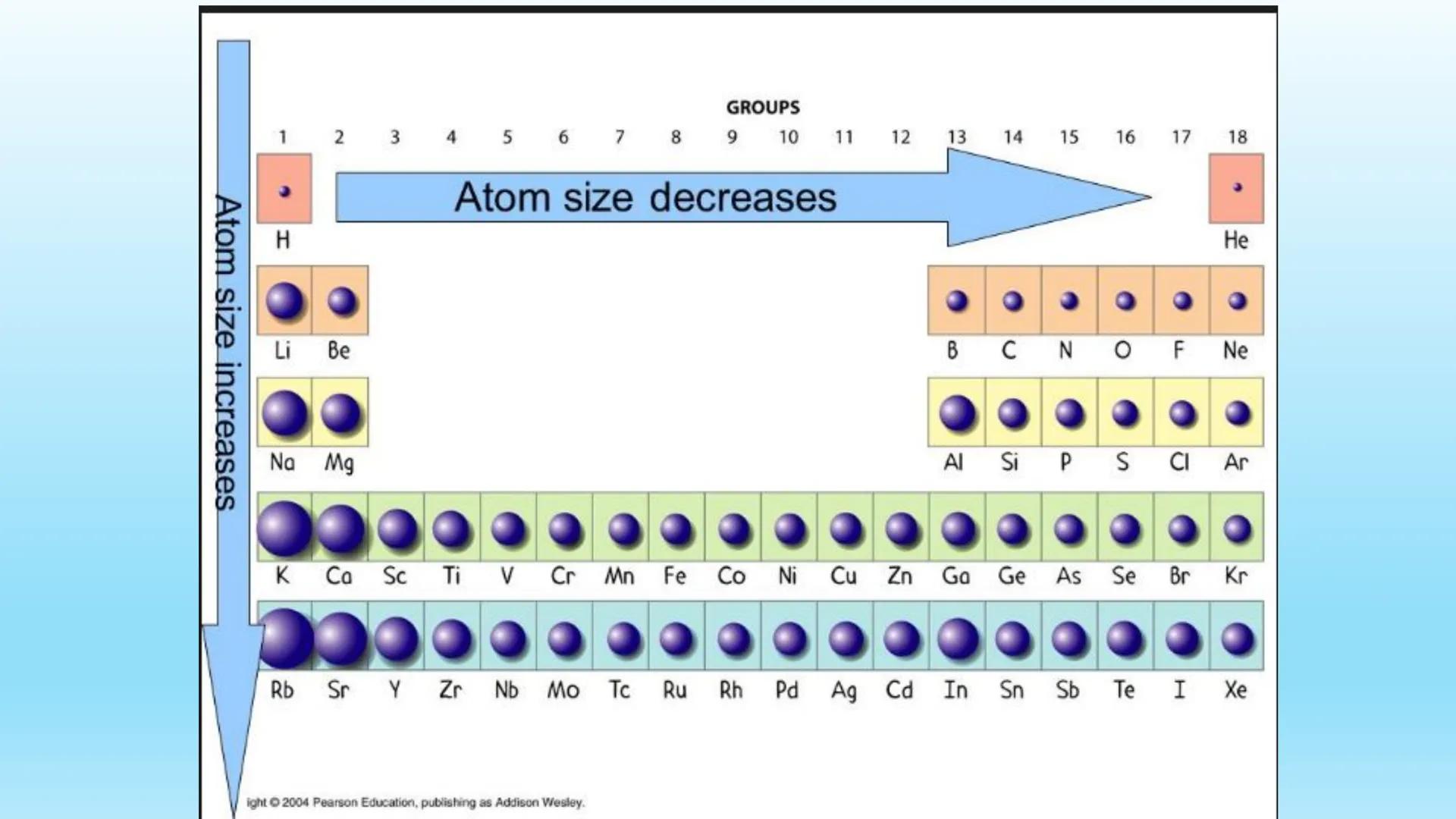
Pe măsură ce ne deplasăm de sus în jos într-o grupă (coloană), mărimea atomilor crește deoarece se adaugă noi straturi electronice. Elementele din partea de jos a tabelului precum Rb, Sr sau Cs au atomi mult mai mari decât "verii" lor din partea superioară.
Când ne deplasăm de la stânga la dreapta într-o perioadă (rând), mărimea atomilor scade treptat. Acest lucru se întâmplă deoarece nucleul devine mai pozitiv și atrage învelișul electronic mai puternic, "comprimând" atomul.
Aplicație practică: Variația razei atomice explică de ce metalele alcaline (Li, Na, K) sunt foarte reactive - au atomi mari cu electroni de valență ușor de cedat, în timp ce gazele nobile (He, Ne, Ar) sunt inerte - au atomi mici cu înveliș electronic complet.
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut: Periodic Table
1Cel mai popular conținut la Chimie
9ALCOOLI
alcooli - materie admitere medicina
Tipuri de reacții chimice
Tipuri de reacții chimice(Reacția de combinare, Reacția de descompunere, Reacția de substituție, Reacția de schimb) + Exemple și Exerciții pe baza lecției
arenele + reacții
lecții arene
Arene
Lectia arene. Reactii si tot ce trebuie stiut pentru bac / admitere
aminoacizi și proteine
aminoacizi și proteine teorie
ZAHARIDE-MONOZAHARIDE SI DIZAHARIDE(fara polizaharide)
Zaharide-monozaharide si dizaharide-pt admitere si bac
Chimie- ALCOOLI
Chimie, alcooli, definitii, proprietati chimice
Formule chimice
spor la învățat
Chimie-Alchene clasa a 10 a
Alchene + reacții
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Proprietățile Elementelor Chimice în Tabelul Periodic
Descoperă cum evoluează proprietățile chimice în tabelul periodic! Vom explora cum dimensiunile atomilor și alte caracteristici ale elementelor se modifică în funcție de poziția lor în sistem, ceea ce ne ajută să înțelegem comportamentul lor chimic.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Variația proprietăților elementelor chimice în tabelul periodic
Tabelul periodic nu este doar o simplă listă de elemente, ci un sistem organizat care ne arată cum se schimbă proprietățile elementelor în mod regulat. Aceste schimbări nu sunt întâmplătoare!
Vom vedea cum caracteristicile atomilor variază pe măsură ce ne deplasăm prin perioade (rânduri) și grupe (coloane) în tabel, făcând chimia mult mai ușor de înțeles și de prezis.
Bine de știut: Înțelegerea modului în care variază proprietățile elementelor în tabelul periodic te va ajuta să prezici comportamentul lor chimic fără să memorezi informații pentru fiecare element în parte!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Proprietățile elementelor chimice
Elementele chimice au două tipuri principale de proprietăți: periodice și neperiodice. Trebuie să le cunoaștem pe ambele pentru a înțelege comportamentul lor!
Proprietățile periodice sunt determinate de configurația electronică și structura învelișului electronic exterior. Acestea variază în mod regulat în tabelul periodic și includ raza atomică, energia de ionizare sau afinitatea pentru electroni.
Proprietățile neperiodice sunt determinate de nucleele atomice și nu urmează un model repetitiv. Cele mai importante sunt numărul atomic (Z) și masa atomică relativă (A), care cresc în general de la un element la altul.
Atenție: Proprietățile periodice sunt cele care ne ajută cel mai mult să înțelegem și să prezicem reactivitatea chimică a elementelor!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Numărul atomic și masa atomică
Numărul atomic (Z) reprezintă proprietatea fundamentală a atomilor și crește cu câte o unitate de la un element la altul în tabelul periodic. Acesta ne arată numărul de protoni din nucleu și determină identitatea elementului.
Masa atomică relativă (A) crește de la primul element până la ultimul din sistem. Inițial, oamenii de știință credeau că masa atomică este proprietatea fundamentală a elementelor.
Mai târziu, s-a descoperit că masa atomică este de fapt o proprietate derivată, care depinde de compoziția izotopică a fiecărui element - adică de amestecul de izotopi cu diferite numere de neutroni.
Interesant: Deși masa atomică crește în general în tabelul periodic, există câteva excepții unde elementul cu Z mai mare are masă atomică mai mică!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Proprietăți fizice periodice
Când explorăm tabelul periodic, putem observa că multe proprietăți fizice se schimbă în mod regulat. Acestea ne ajută să înțelegem comportamentul elementelor!
Printre cele mai importante proprietăți fizice periodice se numără raza atomică și volumul atomic, care ne arată dimensiunea atomilor. De asemenea, avem raza ionică și volumul ionic pentru atomi care au câștigat sau pierdut electroni.
Alte proprietăți esențiale includ energia de ionizare (energia necesară pentru a îndepărta un electron), afinitatea pentru electroni (tendința de a atrage electroni), densitatea și punctele de fierbere și topire.
Aplicație practică: Aceste proprietăți ne ajută să înțelegem de ce unele metale sunt moi (ca sodiul), iar altele sunt dure (ca titanul), sau de ce unele elemente sunt gaze la temperatura camerei, iar altele sunt solide.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Raza atomică
Raza atomică este un concept important, deși în realitate atomii nu au o limită clară ca o bilă solidă. Dimensiunile atomilor se calculează folosind mecanica cuantică și depind de starea în care se află atomul.
Un atom poate avea dimensiuni diferite dacă este izolat (rază atomică) sau legat de alți atomi în molecule (rază covalentă) sau în rețele cristaline (rază metalică sau rază ionică). Aceste diferențe sunt esențiale pentru a înțelege comportamentul chimic al elementelor.
În viziunea mecanicii cuantice, norul electronic al atomului este difuz, fără o limită clară. Totuși, pentru explicarea proprietăților, considerăm raza atomului liber ca fiind distanța de la nucleu până la punctul unde densitatea electronilor este maximă.
Ușor de reținut: Gândește-te la atom ca la un nor difuz de electroni în jurul nucleului, nu ca la o sferă solidă cu margini precise. Raza atomică este doar o convenție utilă!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Raze atomice
Raza atomică se poate măsura în diferite moduri, în funcție de contextul în care se află atomul. Este important să înțelegem aceste diferențe!
Pentru atomii identici legați între ei, raza atomică (r) se definește ca jumătate din distanța (d) dintre nucleele celor doi atomi: r = d/2. Această măsurătoare ne ajută să înțelegem dimensiunea reală a atomilor.
În cazul compușilor ionici, măsurăm suma razelor ionice: raza anionului + raza cationului. Aceasta ne arată distanța dintre nucleele ionilor vecini cu sarcini opuse.
Pentru legăturile covalente, folosim raza covalentă, care reprezintă jumătate din distanța dintre nucleele a doi atomi identici uniți printr-o legătură covalentă.
Aplicație: Când doi atomi diferit formează o legătură, putem aproxima lungimea legăturii adunând razele lor covalente!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Variația razei atomice
Raza atomică se definește practic ca jumătatea distanței dintre nucleele a doi atomi identici vecini din compuși care conțin atomi, nu ioni. Aceasta se determină prin metode cristalografice precise, folosind difracția cu raze X.
Cum variază raza atomică în cadrul unei grupe din tabelul periodic?
- În grupele principale (elementele s și p), razele atomice cresc semnificativ pe măsură ce coborâm în grupă și crește numărul atomic Z
- În grupele secundare (elementele d), razele atomice cresc doar ușor cu Z, existând o diferență mică între elementele din perioadele 5 și 6
Vizualizează: Imaginează-ți că în fiecare grupă, atomii devin ca niște baloane care se umflă treptat pe măsură ce coborâm în tabel, dar elementele tranziţionale se umflă mult mai puțin!

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Variația razei atomice în perioade
Pe măsură ce ne deplasăm de la stânga la dreapta într-o perioadă a tabelului periodic, raza atomică variază în moduri interesante care ne ajută să înțelegem proprietățile elementelor.
În blocul elementelor s și p (grupele principale), razele atomice scad cu creșterea numărului atomic Z. Acest lucru se întâmplă deoarece, deși adăugăm și protoni și electroni, atracția nucleului devine mai puternică și "strânge" norul electronic.
În blocul elementelor d (metalele tranziționale), razele scad de la grupa a 3-a până la grupele 8-10, apoi cresc ușor la elementele din grupele 11-12.
În blocul elementelor f (lantanide și actinide) se observă o scădere ușoară a razelor atomice cu creșterea lui Z, fenomen numit "contracția lantanidelor".
Trucul meu: Pentru a reține tendința generală, gândește-te că în fiecare perioadă, atomii devin tot mai "strânși" pe măsură ce ne deplasăm spre dreapta, până ajungem la gazele nobile.

Înscrie-te pentru a vedea CONȚINUTUL. E gratuit!
- Acces la toate documentele
- Îmbunătățește notele tale!
- Alătură-te milioanelor de elevi
Tabel periodic și variația razei atomice
În tabelul periodic putem observa modele clare de variație a dimensiunii atomilor, care ne ajută să înțelegem și să prezicem proprietățile chimice.
Pe măsură ce ne deplasăm de sus în jos într-o grupă (coloană), mărimea atomilor crește deoarece se adaugă noi straturi electronice. Elementele din partea de jos a tabelului precum Rb, Sr sau Cs au atomi mult mai mari decât "verii" lor din partea superioară.
Când ne deplasăm de la stânga la dreapta într-o perioadă (rând), mărimea atomilor scade treptat. Acest lucru se întâmplă deoarece nucleul devine mai pozitiv și atrage învelișul electronic mai puternic, "comprimând" atomul.
Aplicație practică: Variația razei atomice explică de ce metalele alcaline (Li, Na, K) sunt foarte reactive - au atomi mari cu electroni de valență ușor de cedat, în timp ce gazele nobile (He, Ne, Ar) sunt inerte - au atomi mici cu înveliș electronic complet.
Credeam că nu vei întreba niciodată...
Ce este Companionul AI Knowunity?
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
De unde pot descărca aplicația Knowunity?
Aplicația este disponibilă în Google Play Store și Apple App Store.
Este Knowunity chiar gratuită?
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
Cel mai popular conținut: Periodic Table
1Cel mai popular conținut la Chimie
9ALCOOLI
alcooli - materie admitere medicina
Tipuri de reacții chimice
Tipuri de reacții chimice(Reacția de combinare, Reacția de descompunere, Reacția de substituție, Reacția de schimb) + Exemple și Exerciții pe baza lecției
arenele + reacții
lecții arene
Arene
Lectia arene. Reactii si tot ce trebuie stiut pentru bac / admitere
aminoacizi și proteine
aminoacizi și proteine teorie
ZAHARIDE-MONOZAHARIDE SI DIZAHARIDE(fara polizaharide)
Zaharide-monozaharide si dizaharide-pt admitere si bac
Chimie- ALCOOLI
Chimie, alcooli, definitii, proprietati chimice
Formule chimice
spor la învățat
Chimie-Alchene clasa a 10 a
Alchene + reacții
Cel mai popular conținut
9Eseuri Limba si literatura română
Eseurile sunt structurate dupa barem. Aceste eseuri sunt pentru profilul real, bune si pentru uman dar lipsesc relatiile dintre personaje si caracrerizarile.
Toate eseurile pentru bac
Contin eseul propriu zis si schematizarea acestuia
Eseu”Luceafărul” de Mihai Eminescu complet
eseu
Rezumat ultima noapte de dragoste, întâia de război
Rezumat pe capitole
Eseu-Moara cu noroc ,Ioan Slavici
eseul complet moara cu noroc
Notițe-Bio 11-12
Biologie. Anatomie, fiziologie și genetică
Materie geografie
Bac geografie
Formule pentru subiectul 1 Bac Mate M2
formule pt bac M2 pentru subiectul 1
Eseu- Leoaica tanara, iubirea
Eseu pt bac
Nu găsești ce cauți? Explorează alte MATERII.
Recenzii de la utilizatorii noștri. Ei iubesc să folosească Knowunity — și tu o vei face.
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.