Fenolii reprezintă o clasă importantă de compuși organici aromatici care... Afișează mai mult
Înscrie-te pentru a vedea CONȚINUTULE gratuit!
Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Knowunity AI
Mai mult
Materii
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Afișează toate materiile
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Afișează toate materiile
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Afișează toate materiile
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Afișează toate materiile
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Afișează toate materiile
78
•
Actualizat Mar 30, 2026
•
Maria Alexandra
@mariaalex_f6i03
Fenolii reprezintă o clasă importantă de compuși organici aromatici care... Afișează mai mult
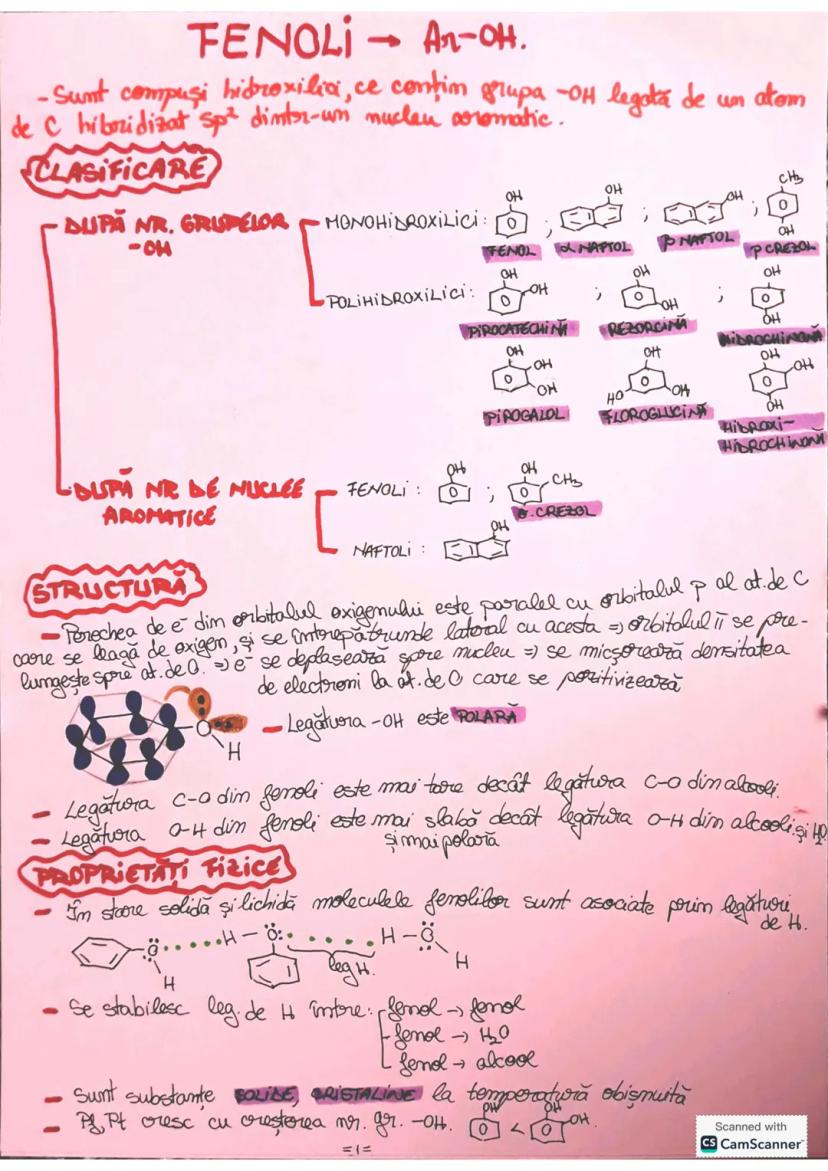





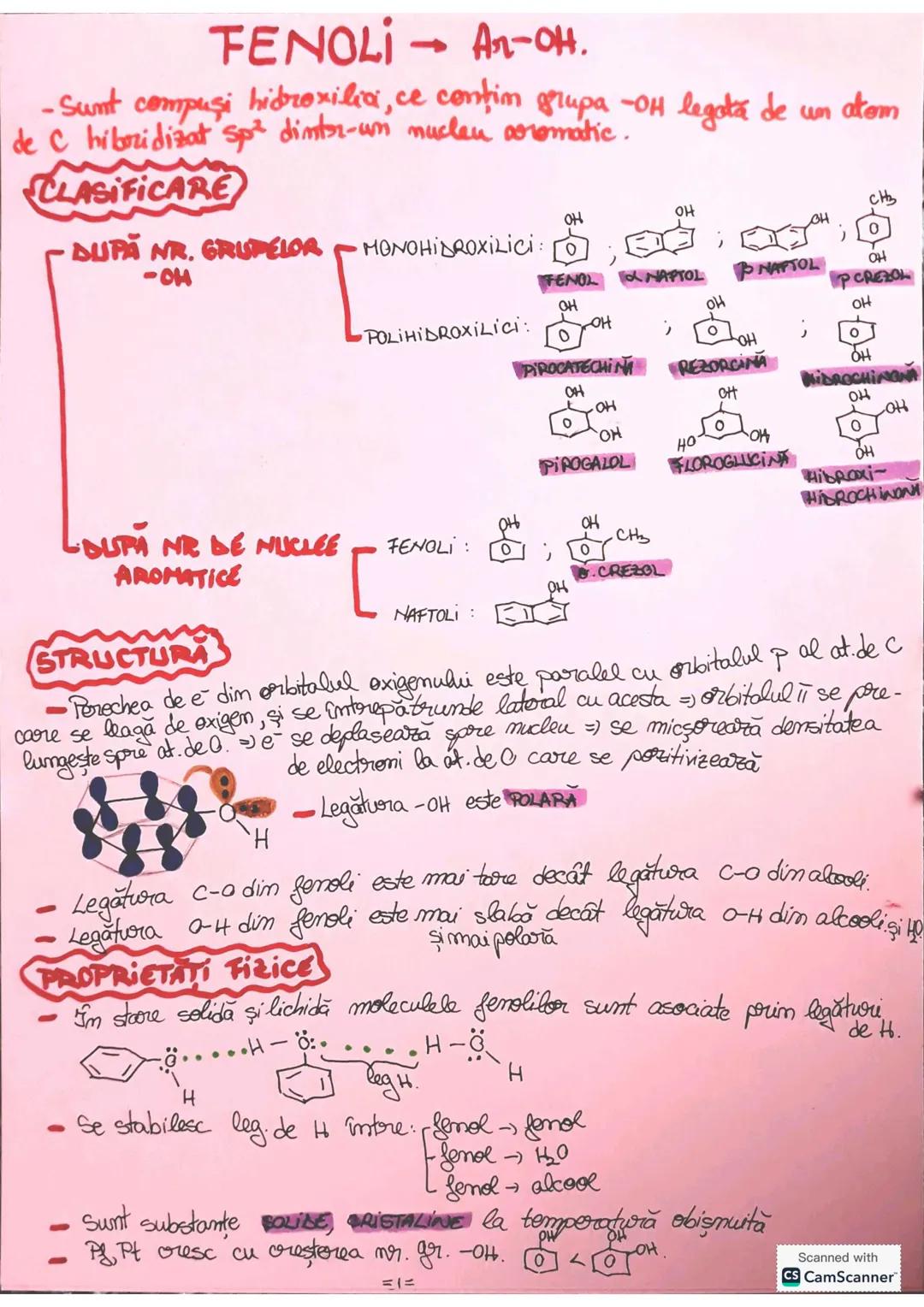
Fenolii sunt compuși hidroxilici în care grupa -OH este legată de un atom de carbon hibridizat sp² dintr-un nucleu aromatic. Structura lor este specială: electronii neparticipanți ai oxigenului interacționează cu sistemul de electroni π al inelului aromatic, mărind stabilitatea legăturii C-O.
Clasificarea fenolilor se poate face după numărul grupelor -OH (monohidroxilici, ca fenolul simplu, sau polihidroxilici, ca pirogaolul) sau după numărul de nuclee aromatice prezente în moleculă.
Legătura O-H din fenoli este mai slabă și mai polară decât în alcooli, în timp ce legătura C-O este mai puternică. Acest lucru influențează direct proprietățile lor fizico-chimice.
💡 Polaritatea crescută a legăturii O-H face fenolii capabili să formeze legături de hidrogen puternice, explicând punctele lor de fierbere ridicate și solubilitatea în apă.
Fenolii sunt, în general, substanțe solide cristaline la temperatura camerei. Punctele de topire și fierbere cresc odată cu numărul grupelor hidroxil din moleculă. În stare solidă și lichidă, moleculele formează rețele de legături de hidrogen între ele sau cu alte substanțe care conțin grupări polare.

Fenolii cu grupe funcționale în pozițiile orto și para, care permit formarea legăturilor de hidrogen, au puncte de fierbere mai scăzute decât izomerii meta. Solubilitatea în apă crește proporțional cu numărul grupelor hidroxil din moleculă.
La expunerea în aer, fenolul se înnegrește datorită proceselor de oxidare. Este higroscopic, toxic și poate provoca arsuri grave la contactul cu pielea. Interesant este că crezolii (derivați metilați ai fenolului) au proprietăți bactericide superioare fenolului simplu.
Din punct de vedere al reactivității chimice, fenolii participă mult mai ușor la reacții de substituție decât benzenul, datorită efectului activator al grupei -OH.
Pentru obținerea fenolilor există mai multe metode:
⚠️ Reacția de hidroliză a derivaților clorurați necesită condiții severe: temperaturi de 300°C și presiuni de 150-200 atmosfere!
Fenolații pot fi hidrolizați în mediu apos, generând fenol și hidroxid de sodiu într-un echilibru chimic.

Fenolii sunt acizi slabi, însă mai puternici decât apa și alcolii. Pe scara acidității, se situează între alcooli și acid cianhidric: alchine < alcoli < apă < fenoli < HCN < acid carbonic.
Caracterul acid al fenolilor se manifestă prin reacții specifice:
Fenolații sunt compuși ionici ușor solubili în apă. În soluție apoasă, fenolatul de sodiu se disociază parțial, dar echilibrul este deplasat spre stânga deoarece fenolul este un acid mai puternic decât apa.
Pentru obținerea eterilor fenolici, fenolații reacționează cu derivați halogenați (de exemplu, cu iodura de metil) sau direct cu oxid de etenă. Fenolii nu se esterifică direct cu alcooli, aceasta fiind o diferență importantă față de acizii carboxilici.
💡 Deși fenolii nu se esterifică direct cu acizii carboxilici, ei pot forma esteri în reacții cu derivați funcționali mai reactivi, precum clorurile acide sau anhidridele acide.
Cu toate acestea, fenolii nu formează esteri în reacție directă cu acizii carboxilici, aceasta fiind o limitare a reactivității lor.

Reacțiile de substituție sunt caracteristice pentru fenoli datorită activării nucleului aromatic de către grupa hidroxil. Grupa -OH direcționează substituenții noi preferențial în pozițiile orto și para.
Halogenarea fenolilor are loc mai ușor decât în cazul benzenului. Se poate realiza cu diverse reactante: Cl₂ în prezența FeCl₃, Br₂ în prezența FeBr₃ sau ICl în prezența HNO₃. Reacția decurge rapid chiar și în condiții blânde.
Nitrarea fenolilor introduce grupa -NO₂ în nucleul aromatic. Aceasta mărește caracterul acid al fenolului, deoarece grupa nitro atrage electroni și stabilizează anionul fenolat rezultat după deprotonare.
Sulfonarea reprezintă introducerea grupei -SO₃H în molecula de fenol. Această reacție are importanță practică pentru obținerea acizilor fenolsulfonici, utilizați în diverse aplicații industriale.
💡 Reactivitatea crescută a fenolilor în reacțiile de substituție se datorează efectului activator și orientor al grupei -OH, care crește densitatea electronică în pozițiile orto și para.
Pe lângă reacțiile de substituție, fenolii pot participa și la reacții de adiție, precum hidrogenarea, deși acestea sunt mai puțin caracteristice pentru compușii aromatici.

Sinteza aspirinei reprezintă un exemplu important de aplicație practică a chimiei fenolilor. Procesul pornește de la fenol, care este transformat prin mai multe etape în acid acetilsalicilic (aspirină).
Prima etapă implică formarea fenolatului de sodiu prin reacția fenolului cu sodiu metalic. Apoi, prin introducerea dioxidului de carbon urmată de acidifiere, se obține acidul salicilic, care conține atât grupa carboxil cât și grupa hidroxil .
În etapa finală, acidul salicilic reacționează cu anhidrida acetică sau acidul acetic pentru a forma acidul acetilsalicilic (aspirina). Această reacție reprezintă o esterificare a grupei hidroxil fenolice.
💡 Aspirina este unul dintre cele mai utilizate medicamente din lume, având efecte antiinflamatoare, analgezice și antipiretice (reduce febra).
Această sinteză ilustrează perfect aplicabilitatea practică a reacțiilor fenolilor în industria farmaceutică. Acidul acetilsalicilic este mai puțin iritant pentru mucoasa gastrică decât acidul salicilic, datorită esterificării grupei hidroxil.

Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
Aplicația este disponibilă în Google Play Store și Apple App Store.
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
App Store
Google Play
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS
Maria Alexandra
@mariaalex_f6i03
Fenolii reprezintă o clasă importantă de compuși organici aromatici care conțin grupa hidroxil (-OH) legată direct de nucleul aromatic. Acești compuși au proprietăți chimice distincte față de alcooli datorită influenței nucleului aromatic asupra grupei hidroxil, ceea ce le conferă un... Afișează mai mult

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Fenolii sunt compuși hidroxilici în care grupa -OH este legată de un atom de carbon hibridizat sp² dintr-un nucleu aromatic. Structura lor este specială: electronii neparticipanți ai oxigenului interacționează cu sistemul de electroni π al inelului aromatic, mărind stabilitatea legăturii C-O.
Clasificarea fenolilor se poate face după numărul grupelor -OH (monohidroxilici, ca fenolul simplu, sau polihidroxilici, ca pirogaolul) sau după numărul de nuclee aromatice prezente în moleculă.
Legătura O-H din fenoli este mai slabă și mai polară decât în alcooli, în timp ce legătura C-O este mai puternică. Acest lucru influențează direct proprietățile lor fizico-chimice.
💡 Polaritatea crescută a legăturii O-H face fenolii capabili să formeze legături de hidrogen puternice, explicând punctele lor de fierbere ridicate și solubilitatea în apă.
Fenolii sunt, în general, substanțe solide cristaline la temperatura camerei. Punctele de topire și fierbere cresc odată cu numărul grupelor hidroxil din moleculă. În stare solidă și lichidă, moleculele formează rețele de legături de hidrogen între ele sau cu alte substanțe care conțin grupări polare.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Fenolii cu grupe funcționale în pozițiile orto și para, care permit formarea legăturilor de hidrogen, au puncte de fierbere mai scăzute decât izomerii meta. Solubilitatea în apă crește proporțional cu numărul grupelor hidroxil din moleculă.
La expunerea în aer, fenolul se înnegrește datorită proceselor de oxidare. Este higroscopic, toxic și poate provoca arsuri grave la contactul cu pielea. Interesant este că crezolii (derivați metilați ai fenolului) au proprietăți bactericide superioare fenolului simplu.
Din punct de vedere al reactivității chimice, fenolii participă mult mai ușor la reacții de substituție decât benzenul, datorită efectului activator al grupei -OH.
Pentru obținerea fenolilor există mai multe metode:
⚠️ Reacția de hidroliză a derivaților clorurați necesită condiții severe: temperaturi de 300°C și presiuni de 150-200 atmosfere!
Fenolații pot fi hidrolizați în mediu apos, generând fenol și hidroxid de sodiu într-un echilibru chimic.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Fenolii sunt acizi slabi, însă mai puternici decât apa și alcolii. Pe scara acidității, se situează între alcooli și acid cianhidric: alchine < alcoli < apă < fenoli < HCN < acid carbonic.
Caracterul acid al fenolilor se manifestă prin reacții specifice:
Fenolații sunt compuși ionici ușor solubili în apă. În soluție apoasă, fenolatul de sodiu se disociază parțial, dar echilibrul este deplasat spre stânga deoarece fenolul este un acid mai puternic decât apa.
Pentru obținerea eterilor fenolici, fenolații reacționează cu derivați halogenați (de exemplu, cu iodura de metil) sau direct cu oxid de etenă. Fenolii nu se esterifică direct cu alcooli, aceasta fiind o diferență importantă față de acizii carboxilici.
💡 Deși fenolii nu se esterifică direct cu acizii carboxilici, ei pot forma esteri în reacții cu derivați funcționali mai reactivi, precum clorurile acide sau anhidridele acide.
Cu toate acestea, fenolii nu formează esteri în reacție directă cu acizii carboxilici, aceasta fiind o limitare a reactivității lor.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Reacțiile de substituție sunt caracteristice pentru fenoli datorită activării nucleului aromatic de către grupa hidroxil. Grupa -OH direcționează substituenții noi preferențial în pozițiile orto și para.
Halogenarea fenolilor are loc mai ușor decât în cazul benzenului. Se poate realiza cu diverse reactante: Cl₂ în prezența FeCl₃, Br₂ în prezența FeBr₃ sau ICl în prezența HNO₃. Reacția decurge rapid chiar și în condiții blânde.
Nitrarea fenolilor introduce grupa -NO₂ în nucleul aromatic. Aceasta mărește caracterul acid al fenolului, deoarece grupa nitro atrage electroni și stabilizează anionul fenolat rezultat după deprotonare.
Sulfonarea reprezintă introducerea grupei -SO₃H în molecula de fenol. Această reacție are importanță practică pentru obținerea acizilor fenolsulfonici, utilizați în diverse aplicații industriale.
💡 Reactivitatea crescută a fenolilor în reacțiile de substituție se datorează efectului activator și orientor al grupei -OH, care crește densitatea electronică în pozițiile orto și para.
Pe lângă reacțiile de substituție, fenolii pot participa și la reacții de adiție, precum hidrogenarea, deși acestea sunt mai puțin caracteristice pentru compușii aromatici.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Sinteza aspirinei reprezintă un exemplu important de aplicație practică a chimiei fenolilor. Procesul pornește de la fenol, care este transformat prin mai multe etape în acid acetilsalicilic (aspirină).
Prima etapă implică formarea fenolatului de sodiu prin reacția fenolului cu sodiu metalic. Apoi, prin introducerea dioxidului de carbon urmată de acidifiere, se obține acidul salicilic, care conține atât grupa carboxil cât și grupa hidroxil .
În etapa finală, acidul salicilic reacționează cu anhidrida acetică sau acidul acetic pentru a forma acidul acetilsalicilic (aspirina). Această reacție reprezintă o esterificare a grupei hidroxil fenolice.
💡 Aspirina este unul dintre cele mai utilizate medicamente din lume, având efecte antiinflamatoare, analgezice și antipiretice (reduce febra).
Această sinteză ilustrează perfect aplicabilitatea practică a reacțiilor fenolilor în industria farmaceutică. Acidul acetilsalicilic este mai puțin iritant pentru mucoasa gastrică decât acidul salicilic, datorită esterificării grupei hidroxil.

Acces la toate documentele
Îmbunătățește notele tale!
Alătură-te milioanelor de elevi
Companionul nostru AI este creat special pentru nevoile studenților. Bazându-ne pe milioanele de materiale de pe platformă, putem oferi răspunsuri exacte și relevante pentru studenți. Dar nu este vorba doar despre răspunsuri, companionul este mai ales despre ghidarea studenților prin provocările zilnice de învățare, cu planuri de studiu personalizate, chestionare sau conținuturi în chat și personalizare 100% bazată pe abilitățile și evoluțiile studenților.
Aplicația este disponibilă în Google Play Store și Apple App Store.
Da! Bucură-te de access la materiale de studiu, conectează-te cu alți elevi, și primește ajutor instant - toate acestea la un click distanță. În plus, câștigă puncte ca să deblochezi mai multe funcționalități!
0
Instrumente inteligente NOU
Transformă această notiță în: ✓ 50+ întrebări de exersare ✓ Flashcard-uri interactive ✓ Examen de practică complet ✓ Planuri de eseu
App Store
Google Play
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS
Aplicația este foarte ușor de utilizat și bine concepută. Am găsit tot ce căutam până acum și am reușit să învăț multe din prezentări! Cu siguranță voi folosi aplicația pentru o temă la clasă! Și desigur, ajută mult ca sursă de inspirație.
Ștefan S
utilizator iOS
Această aplicație este super. Sunt atât de multe materiale de studiu și ajutor pentru elevi [...]. Materia mea mai problematică este franceza, de exemplu, și aplicația oferă foarte multe materiale ajutătoare. Mulțumită acestei aplicații, mi-am îmbunătățit franceza. Aș recomanda-o oricui.
Samantha Klich
utilizator Android
Wow, sunt cu adevărat impresionat. Am încercat aplicația pentru că am văzut-o promovată de multe ori și am rămas uimit. Aceasta este AJUTORUL de care ai nevoie pentru școală și, mai presus de toate, oferă atât de multe lucruri, precum exerciții și fișe de informații, care mi-au fost FOARTE de ajutor.
Anna
utilizator iOS
Te ajută să înveți foarte repede și ști foarte bine ce ai dori tu să înveți, vă recomand cu drag să încercați și să învățați mai repede.!
Thomas R
utilizator iOS
Foarte bună aplicația!!!! Mă ajută să înțeleg mult mai bine lecțiile și temele le termin mult mai repede.👍❤️
Paul P
utilizator Android
Te ajută foarte bine la teme acest robot,recomand!
David K
utilizator iOS
Aplicația e grozavă! Tot ce trebuie să fac este să introduc subiectul în bara de căutare și primesc răspunsul foarte rapid. Nu mai trebuie să mă uit la 10 videoclipuri pe YouTube pentru a înțelege ceva, deci îmi economisesc timpul. Super recomandat!
Sudenaz Ocak
utilizator Android
La școală eram chiar slab la matematică, dar datorită aplicației, mă descurc mai bine acum. Sunt atât de recunoscător că ai creat aplicația.
Greenlight Bonnie
utilizator Android
Această aplicație e super interesantă și seamănă ca tiktok-ul doar că tu ai doar teorie și explicații.
Karla S
utilizator Android
Nu mai trebuie să stau cu orele să învăț după caiet când pot să citesc de 2 ori lecțiile care apar aici și iau 10 la test ! Knowunity m-a ajutat să iau nota 9,20 la română ! Voi recomanda ff tare aceasta aplicate , să nu uităm ca are și chat GPT !👍🏻
Denisa B
utilizator iOS
CHESTIONARELE ȘI FLASHCARD-URILE SUNT ATÂT DE UTILE ȘI IUBESC Knowunity AI. E LITERALMENTE CA CHATGPT DOAR CĂ MAI DEȘTEPT!! M-A AJUTAT ȘI CU PROBLEMELE MELE CU MASCARA!! PLUS CU MATERIILE MELE ADEVĂRATE! EVIDENT 😍😁😲🤑💗✨🎀😮
Sarah L
utilizator Android
Este foarte bună te ajută la teme te face să înțelegi lecțiile am înțeles o lecție în 20 de minute i singură nu reușeam să o învăț dar cu Knowunity am învățat-o foarte ușor
Alessia V
utilizator iOS